Granulocytær anaplasmose hos hund
Granulocytær anaplasmose er en vektorbåren infeksjon som overføres via flått. Hos hund gir infeksjonen lite spesifikke kliniske tegn som redusert allmenntilstand, redusert matlyst, feber og muskel- og skjelettsmerter. De vanligste og mest spesifikke hematologiske avvikene er trombocytopeni av varierende alvorlighetsgrad og påvisning av intracytoplasmatiske morulaer i granulocytter i blodutstryk. Ved biokjemisk analyse ses ofte økte akuttfaseproteiner forenlig med systemisk inflammasjon. Respons på behandling med antibiotika er som oftest rask og prognosen ansett som god.
Veterinær, EMSAVM – Neurology, Spesialistkandidat i smådyrsykdommer, hund og katt, AniCura Jeløy Dyresykehus
Veterinær, MS Clinical Companion Animal Science Oncology, Spesialist i smådyrsykdommer, hund og katt,
Dyreklinikken Son
Veterinær, MANZCVS ECC, Fredrikstad Dyrehospital
Veterinær, Ph.d, Dip.ECVCP, NMBU Veterinærhøgskolen
Innledning
Granulocytær anaplasmose er en vektorbåren sykdom som finnes utbredt over hele verden (1,2). Den ansvarlige organismen, Anaplasma phagocytophilum, er en gram-negativ, obligat intracellulær alfaproteobakterie som invaderer granulocytter der de utvikles og samles i små grupper (morulaer) (1-3). Bakterien overføres ved hjelp av en vektor, som oftest flått i slekten Ixodes, og kan gi sykdom hos flere typer pattedyr som hunder, katter, hester, domestiserte og ville drøvtyggere og mennesker (1,3). I Norge og resten av Europa er den viktigste vektoren for A. phagocytophilum skogflåtten Ixodes ricinus (2). Bakterien har transstadial overføring i vektoren (4), og studier har vist at forekomsten i skogflått undersøkt ulike steder i Norge (Viken, Telemark, Sørlandet) er fra 1,4 % til 8,0 % (5-7). Granulocytær anaplasmose er en zoonose, men sykdommen smitter ikke direkte fra dyr til mennesker. Sykdommen hos mennesker er oftest asymptomatisk eller mild, og det var frem til 2018 rapportert ni tilfeller i Norge (8).
A. phagocytophilum kan gi akutt sykdom hos hund med feber, redusert allmenntilstand, anoreksi og smerter i muskler og skjelett. Vanlige hematologiske og biokjemiske endringer inkluderer trombocytopeni, anemi, påvisning av intracytoplasmatiske morulaer i granulocytter ved undersøkelse av blodutstryk, økte leverenzymer, hypoalbuminemi og hyperbilirubinemi (1,3). Det finnes flere kommersielt tilgjengelige antistofftester som kan brukes diagnostisk, men på grunn av infeksjonens akutte forløp, vil mange hunder kunne ha et lavt antistofftiter på testtidspunktet og et negativt testresultat (3). I tidlige stadier av sykdommen, vil en PCR-undersøkelse for Anaplasma spp. DNA i blodet ofte være positiv, også hos hunder som er negative på de kvalitative antistofftestene som benyttes i klinikken (3).
Forekomsten av klinisk sykdom ved smitte med A. phagocytophilum hos hund i Norge er ikke kjent. I denne kasusserien presenteres kliniske tegn, diagnostikk og behandling av fire hunder med granulocytær anaplasmose.
Kasusserie
Fire hunder som ble diagnostisert med A. phagocytophilum infeksjon i perioden september 2020 til mai 2025 ble inkludert.
Kasus I
Signalement og anamnese
En strihåret vorstehhund, kastrert tispe på 7 år veide 24,4 kg. Hunden hadde blitt importert til Norge fra Danmark som valp, men hadde ikke vært utenlands siden. Flåttprofylakse hadde blitt administrert jevnlig gjennom sesongen, men eier hadde observert en flått på hunden en og en halv uke tidligere. Hunden hadde ingen kjent sykdom og ble ikke behandlet med noen legemidler utover flåttprofylakse. Eier var usikker på når hunden sist var vaksinert. Hunden hadde vært slapp i et par dager, hadde dårlig appetitt og eier hadde observert en svært mørk, nærmest sort avføring med normal konsistens. Det var ikke observert oppkast, men hunden hadde av og til siklet og gulpet.
Ved undersøkelse hos veterinær ble det avdekket feber (40,7 °C) og markert trombocytopeni (15 x 109/L; RI: 200 – 460 x 109/L). Hunden fikk 200 mL RingerAcetat iv før den i september 2020 ble henvist til AniCura Jeløy Dyresykehus for utredning av trombocytopeni.
Klinisk undersøkelse
Ved klinisk undersøkelse var hunden nedstemt. Slimhinnene var rosa, tørre og klebrige med en kapillærfylningstid (KFT) på to og ett halvt sekund. Femoralpulsen var av god kvalitet, synkron med hjerteslagene og med en frekvens på 80/min. Respirasjonsfrekvensen var 24/min, og hunden hadde et kostoabdominalt respirasjonsmønster. Auskultasjon av hjerte og lunger var uten anmerkning, og det var ingen avvik ved palpasjon av buken. Tilgjengelige lymfeknuter var symmetriske med normal størrelse og tekstur. Hunden hadde ingen tegn til blødninger i hud, slimhinner eller ledd og rektaltemperaturen ble målt til 40,5 °C. Det ble ikke observert makroskopisk synlig blod i avføringen ved rektalundersøkelse.
Diagnostiske undersøkelser
Den markerte trombocytopenien påvist hos henvisende veterinær var ikke bekreftet med morfologisk undersøkelse. Det var derfor ønskelig å verifisere denne før undersøkelser med hensyn på årsakssammenheng ble utført.
Hematologiske og biokjemiske analyser ble utført på henholdsvis Siemens Advia 2120i og Siemens Advia 1800 (Tabell 1, Kasus I, Dag 0). Signifikante avvik inkluderte en markert trombocytopeni og en markert økning i C-reaktivt protein (CRP). Det ble også påvist en mild nøytropeni og en mild lymfopeni. Morfologisk undersøkelse av blodutstryk ble utført av klinisk patolog med funn av en mild nøytropeni med mild venstreforskyvning og påvisning av multiple, større plateklumper, slik at platetallet var høyere enn telletallet fra automatisert analyse. I flere nøytrofile granulocytter var det basofile legemer forenlig med morulaer, høyst suspekt med henblikk på infeksjon med A. phagocytophilum.
Det ble også utført en hurtigtest for vektorbårne infeksjoner (IDEXX SNAP 4Dx Plus) som var negativ for Anaplasma spp. (A. phagocytophilum, Anaplasma platys), Ehrlichia spp. (Ehrlichia canis, Ehrlichia ewingii), Borrelia burgdorferi og Diriofilaria immitis.
Det ble utført måling av urinens spesifikke vekt og kjemisk analyse med urinstiks (IDEXX VetUA) i skålurin. Urinen var konsentrert med en spesifikk vekt på 1,045 og urinstiks viste utslag på protein (5,0 g/L, 3+) og blod (50 erytrocytter/µL, 3+).
Røntgenbilder av thorax i tre plan var uten synlige avvik. En ultralydundersøkelse av abdomen ble utført på usedert pasient og avdekket mild lymfadenomegali i krøslymfeknuter, samt mild splenomegali.
Analytt |
Kasus I |
Kasus II |
Kasus III |
RI |
Kasus IV |
RI |
|||||
|---|---|---|---|---|---|---|---|---|---|---|---|
Dag 0 |
Dag 6 |
Dag 0 |
Dag 9 |
Dag 0 |
Dag 4 |
Advia 2120i |
Dag 0 |
Dag 12 |
ProCyte |
||
RBC |
5,6 |
6,3 |
6,1 |
6,4 |
5,3 |
5,7 |
5,1-8,5x1012/L |
6,02 |
7,15 |
5,65-8,87x1012/L |
|
HCT |
0,39 |
0,45 |
0,40 |
0,42 |
0,37 |
0,41 |
0,35-0,55 L/L |
35,2 |
44,8 |
37,3-61,7 % |
|
HGB |
136 |
152 |
151 |
149 |
130 |
136 |
120-180 g/L |
13,5 |
16,2 |
13,1-20,5 g/dL |
|
MCV |
69,8 |
71,9 |
65,7 |
65,8 |
70,2 |
71,1 |
62,0-76,0 fL |
58,5 |
62,7 |
61,6-73,5 fL |
|
MCHC |
346 |
339 |
379 |
356 |
351 |
334 |
320-360 g/L |
38,4 |
36,2 |
32,0-37,9 g/dL |
|
RDW |
12,2 |
12,2 |
12,8 |
13,8 |
12,5 |
12,5 |
11,0-16,0 % |
15,4 |
19,0 |
13,6-21,7 % |
|
RETIC |
7 |
35 |
14 |
50 |
6 |
9 |
8-129x109/L |
9,6 |
170,2 |
10,0-110,0 K/µL |
|
WBC |
4,0 |
5,3 |
5,6 |
8,7 |
11,6 |
26,0 |
6,0-18,0x109/L |
6,37 |
8,53 |
5,05-16,76x109/L |
|
NEUT |
2,9 1) 2) |
3,2 |
4,3 2) |
5,4 |
8,6 1) 2) |
19,5 4) |
3,6-13,0x109/L |
5,75 1) 2) |
5,43 |
2,95-11,64x109/L |
|
LYMPH |
0,7 |
1,5 |
0,9 |
2,5 |
1,5 |
4,6 |
0,8-5,8x109/L |
0,29 |
1,94 |
1,05-5,10x109/L |
|
MONO |
0,2 |
0,3 |
0,2 |
0,4 |
0,7 |
1,2 |
0-1,6x109/L |
0,32 |
0,50 |
0,16-1,12x109/L |
|
EOS |
0 |
0,2 |
0,1 |
0,3 |
0 |
0,1 |
0-1,8x109/L |
0,00 |
0,61 |
0,06-1,23x109/L |
|
BASO |
0 |
0 |
0 |
0 |
0,1 |
0,2 |
0-0,4x109/L |
0,01 |
0,05 |
0-0,10x109/L |
|
LUC |
0,3 |
0 |
0 |
0 |
0,7 |
0,4 |
0-1,5x109/L |
- |
- |
- |
|
PLT |
11 3) |
239 |
60 |
206 |
16 |
92 |
180-500x109/L |
65 |
386 |
148-484 K/µL |
|
MPV |
28,7 |
15,2 |
13,6 |
11,6 |
24 |
21,3 |
8,4-14,1 fL |
14,9 |
11,6 |
8,7-13,2 fL |
|
PCT |
0,03 |
0,36 |
0,08 |
0,24 |
0,04 |
0,20 |
0,10-0,40 % |
0,10 |
0,45 |
0,14-0,46 % |
|
Advia 1800 |
Catalyst One |
||||||||||
CRP |
140,9 |
13,8 |
103,4 |
14,9 |
124,4 |
37,5 |
0-15,0 mg/L |
89,3 |
9,6 |
0-10,0 mg/L |
|
1 Mild venstreforskyvning.
2 Påvisning av morulaer.
3 Påvist plateklumper i blodutstryk, reelt platetall er høyere enn telletallet fra automatisert analyse.
4 Påvisning av et lavt antall morulaer.
Diagnose og behandling
I påvente av svar på innledende diagnostiske undersøkelser ble pasienten behandlet med RingerAcetat (Fresenius Kabi) 5 mL/kg/time iv, paracetamol (Paracet, Weifa) 10 mg/kg bid po og maropitant (Prevomax, Dechra) 1 mg/kg sid iv.
Kliniske og diagnostiske funn var forenlige med granulocytær anaplasmose. Behandling med antibiotika, doksysyklin (Doxylin, Actavis) 10 mg/kg bid po i 14 dager ble igangsatt og hunden ble sendt hjem etter ett døgns hospitalisering. På dette tidspunktet var hunden betydelig kvikkere, afebril og spiste med god appetitt.
Oppfølging
Hunden kom til kontroll seks dager etter hjemsendelse og eier opplevde da hunden som helt frisk igjen. Det var ingen avvik ved klinisk undersøkelse. Hematologiske og biokjemiske analyser viste at blodplater og CRP nå var innenfor sine respektive referanseintervaller (Tabell 1, Kasus I, Dag 6). Det ble også utført en ny morfologisk undersøkelse som verifiserte telletallene, og morulaer ble ikke identifisert. Responsen på behandlingen med doksysyklin ble vurdert som svært god, og planlagt behandling ble anbefalt fullført.
Kasus II
Signalement og anamnese
En strihåret dachshund, kastrert tispe på 4,5 år veide 11,8 kg. Hunden hadde aldri vært på utenlandsreise, fikk regelmessig profylaktisk behandling mot flått og det var ikke nylig observert flått på hunden. Den hadde ikke kjent sykdom med unntak av en litt “sensitiv tarm”, og ble fôret med et spesialfôr (Hill’s Prescription Diet i/d Stress) for dette. Hunden hadde ikke fått legemidler utover flåttprofylakse og anbefalte vaksiner. Hunden var slapp hjemme og ville hverken spise eller drikke. Eier hadde målt en rektaltemperatur på 40,2 °C. Det var ikke observert oppkast, men avføringen hadde hatt varierende konsistens og hunden spiste store mengder med gress. Eier syntes det virket som om hunden hadde ubehag ved urinering. Det var ikke observert blod i urinen eller avføringen. Hunden kom i juli 2023 til AniCura Jeløy Dyresykehus grunnet redusert allmenntilstand og feber.
Klinisk undersøkelse
Hunden var tydelig nedstemt ved innledende undersøkelse. Slimhinnene var rosa og mildt klebrige med en KFT på to sekunder. Femoralpulsen var av god kvalitet, synkron med hjerteslagene og med en frekvens på 104/min. Respirasjonsfrekvensen var 28/min. Hunden hadde et kostoabdominalt respirasjonsmønster, avbrutt av intermitterende pesing. Auskultasjon av hjerte og lunger var uten anmerkning. Tilgjengelige lymfeknuter var symmetriske med normal størrelse og tekstur. Ved palpasjon av buken virket hunden øm, spesielt ved kaudal palpasjon, men uten andre funn. Det ble observert markert bilateral blefarospasme og skleral karinjeksjon som var mest uttalt i limbus. Ved øyeundersøkelse ble det påvist redusert trykk (9-10 mmHg; RI: 15-25) i begge øyne, mens undersøkelse av retina var uten anmerkning. Ved mønstring ble det ikke observert halthet, men generelt stive bevegelser og ved manipulasjon av hasene viste hunden tegn til smerte. Bevegelsessystemet var ellers uten anmerkning. Hunden hadde ingen blødninger i hud eller slimhinner og rektaltemperatur ble målt til 40,4 °C. Det ble ikke observert makroskopisk synlig blod i avføringen ved rektalundersøkelse.
Diagnostiske undersøkelser
Hematologiske og biokjemiske analyser ble utført på henholdsvis Siemens Advia 2120i og Siemens Advia 1800 (Tabell 1, Kasus II, Dag 0). Signifikante avvik inkluderte moderat til markert trombocytopeni og markert økning i CRP.
Ultralydundersøkelse av abdomen ble utført uten signifikante funn. Urinprøve ble tatt ved cystocentese i forbindelse med ultralydundersøkelsen. Det ble målt spesifikk vekt og utført kjemisk analyse med urinstiks (IDEXX VetUA). Urinen hadde spesifikk vekt på 1,011 etter behandling med intravenøs væske, og urinstiks viste utslag på blod (250 erytrocytter/µL, 4+). Bakteriologisk dyrkning av urinen ble utført uten at bakterier ble påvist. En hurtigtest for vektorbårne infeksjoner (IDEXX Snap 4Dx Plus) var positiv for Anaplasma spp. og negativ for Ehrlichia spp., B. burgdorferi og D. immitis.
Morfologisk undersøkelse av blodutstryk ble utført eksternt (IDEXX Laboratories). Det ble påvist moderat til markert trombocytopeni og morulaer i nøytrofile granulocytter, høyst suspekt med henblikk på infeksjon med A. phagocytophilum. Det ble også utført kvantifisering av antistoffer i serum ved hjelp av ELISA som viste 50,3 TU (RI: 0-8), og PCR-undersøkelse for Anaplasma spp. på EDTA-stabilisert fullblod som var positiv.
Diagnose og behandling
I påvente av svar på innledende diagnostiske undersøkelser ble pasienten hospitalisert på klinikken og behandlet med RingerAcetat, (Fresenius Kabi) 5,5 mL/kg/time iv, paracetamol (Paracet, Weifa) 10 mg/kg bid po og maropitant (Prevomax, Dechra) 1 mg/kg sid iv.
Kliniske og diagnostiske funn var forenlige med granulocytær anaplasmose. Behandling med doksysyklin (Ronaxan vet. Boehringer Ingelheim) 8,8 mg/kg bid po i 28 dager ble igangsatt. Hunden ble sendt hjem etter hospitalisering i ett døgn. På dette tidspunktet var hunden betydelig kvikkere, afebril og spiste med god appetitt.
Oppfølging
Hunden kom til kontroll ni dager etter hjemsendelse. Eier opplevde da hunden som betydelig bedre, men fremdeles litt slappere enn normalt. Det var ingen signifikante avvik ved klinisk undersøkelse.
Nye hematologiske og biokjemiske analyser viste blodplater og CRP innenfor sine respektive referanseintervaller (Tabell 1, Kasus II, Dag 9). Morfologisk undersøkelse ble ikke utført.
Hunden kom deretter til kontroll tre uker etter oppstart av behandling. Eier opplevde da hunden som frisk, og den kliniske undersøkelsen var uten avvik. Respons på behandlingen ble vurdert som svært god, og den foreskrevne behandlingen ble anbefalt fullført. En ny PCR- undersøkelse for Anaplasma spp. på EDTA-stabilisert fullblod var negativ. Nytt kvantitativt antistofftiter ble analysert etter åtte måneder og viste et resultat på 7,2 TU (RI: 0-8).
Kasus III
Signalement og anamnese
En dvergpuddel, intakt hannhund på 11 år veide 6,2 kg. Hunden hadde vært jevnlig i Sverige (Stockholm og Fjällbacka) gjennom sommeren, men det var over fire måneder siden siste reise. Flåttprofylakse hadde blitt jevnlig administrert i løpet av sesongen. Det var ikke nylig observert flått på hunden. Hunden hadde ingen kjent sykdom og fikk ingen legemidler utover profylaktisk behandling mot flått og anbefalte vaksiner.
Hunden hadde i fire dager vist redusert allmenntilstand og svært redusert appetitt. Det var ikke observert oppkast eller unormal avføring. Ved undersøkelse hos veterinær ble det påvist feber (39,8 °C), samt et sår i munnhulen etter tanntrekk utført noen måneder tidligere. Hunden ble behandlet med paracetamol og amoxicillin, men ble allment dårligere i løpet av de neste dagene. Videre undersøkelse to dager senere avdekket høyere feber (40,5 °C), et lavt antall blodplater (37 K/µL; RI: 148-484 K/µL) og økt CRP (>100 mg/L; RI: 0-10 mg/L). Andre biokjemiske analyser var uten signifikante avvik.
Behandling med meloksikam og klindamycin ble igangsatt uten bedring, og hunden ble henvist til AniCura Jeløy Dyresykehus i november 2024 for videre utredning av feber og trombocytopeni.
Klinisk undersøkelse
Hunden fremsto slapp og nedstemt ved ankomst til dyresykehuset. Slimhinnene var rosa og klebrige med KFT på to sekunder. Femoralpulsen var av god kvalitet, synkron med hjerteslagene med en frekvens på 84/min. Respirasjonsfrekvensen var 24/min, og hunden hadde et kostoabdominalt respirasjonsmønster. Auskultasjon av hjerte og lunger var uten anmerkning og tilgjengelige lymfeknuter var symmetriske med normal størrelse og tekstur. Abdominal palpasjon var uten tydelige avvik, men hunden reagerte noe ved kaudal palpasjon. I munnhulen var det et sår i området for tann 203 etter tidligere tanntrekk. Hunden hadde ingen tegn til blødninger i hud, slimhinner eller ledd og rektaltemperaturen ble målt til 39,7 °C. Det ble ikke observert makroskopisk synlig blod i avføringen ved rektalundersøkelse.
Diagnostiske undersøkelser
Ved ankomst ble det utført hematologiske analyser og analyse av CRP på henholdsvis Siemens Advia 2120i og Siemens Advia 1800 som viste en markert trombocytopeni og en markert økning i CRP (Tabell 1, Kasus III, Dag 0).
Morfologisk undersøkelse av blodutstryk ble utført av klinisk patolog med funn av markert trombocytopeni og mild venstreforskyvning av nøytrofile granulocytter. I flere nøytrofile granulocytter var det basofile legemer forenlig med morulaer (Figur 1), høyst suspekt med henblikk på infeksjon med A. phagocytophilum. Det ble også utført en hurtigtest for vektorbårne infeksjoner (IDEXX Snap 4dx Plus) som var negativ.
I kateterurin ble det målt spesifikk vekt, samt utført kjemiske analyser med urinstiks (IDEXX VetUA). Urinen hadde en spesifikk vekt på 1,010 etter behandling med intravenøs væske, og urinstiks viste utslag på protein (0,3 g/L, 1+) og blod (250 erytrocytter/µL, 4+).
En PCR-undersøkelse for Anaplasma spp. ble utført på EDTA-stabilisert fullblod ved eksternt laboratorium (IDEXX Laboratories), og var positiv.

Figur 1. Nøytrofil granulocytt med morula i cytoplasma. Det kan også påvises redusert tetthet av plater. Modifisert Wright’s farging. 40x objektiv.
Foto: Bente Kristin Sævik
Diagnose og behandling
I påvente av svar på innledende diagnostiske undersøkelser ble pasienten hospitalisert med følgende behandling; RingerAcetat (Fresenius Kabi) 3,3 mL/kg/time iv, paracetamol (Paracet, KaroPharma) 10 mg/kg bid po og maropitant (Vominil, VetVivaRichter) 1 mg/kg sid iv.
Kliniske og diagnostiske funn var forenlige med granulocytær anaplasmose og behandling med doksysyklin (Ronaxan vet. Boehringer Ingelheim) 8 mg/kg bid po i 21 dager ble igangsatt. Hunden ble sendt hjem etter hospitalisering i ett døgn. Ved hjemsendelsen var hunden betydelig kvikkere og afebril, men hadde fremdeles noe redusert appetitt.
Oppfølging
Hunden kom til en kontroll fire dager etter hjemsendelse. Eier opplevde da hunden som betydelig bedre. Matlysten var mye bedre, men hunden var fremdeles noe slapp. Det var ingen signifikante avvik ved klinisk undersøkelse.
Nye hematologiske og biokjemiske analyser viste en økning i blodplater verifisert ved morfologisk undersøkelse og en reduksjon i CRP (Tabell 1, Kasus III, Dag 4). Morulaer var fremdeles til stede i et lavt antall nøytrofile granulocytter. Ved ny kontroll 16 dager etter hjemsendelse var både antall blodplater og CRP innenfor sine respektive referanseintervaller. Morulaer ble ikke identifisert. Respons på behandling ble vurdert som svært god, og den igangsatte behandlingen ble anbefalt fullført.
Kasus IV
Signalement og anamnese
En tibetansk spaniel, intakt hannhund på 10 år veide 6,8 kg. Hunden hadde aldri vært på utenlandsreise, fikk regelmessig profylaktisk behandling mot flått med fluralaner i tablettform (Bravecto, MSD Animal Health), og det var ikke nylig observert flått på hunden. Den hadde ikke kjent sykdom og fikk ingen legemidler utover flåttprofylakse og anbefalte vaksiner. Hunden hadde hatt anoreksi i ett døgn. Hunden var slapp hjemme og ville heller ikke drikke. Det var ikke observert oppkast eller diaré. Det var ikke observert blod i urin eller avføring. På grunn av den nedsatte allmenntilstanden kom hunden i mai 2025 til AniCura Jeløy Dyresykehus.
Klinisk undersøkelse
Hunden fremsto som relativt kvikk ved ankomst til dyresykehuset. Slimhinnene var rosa og fuktige med en KFT på under to sekunder. Femoralpulsen var av god kvalitet, synkron med hjerteslagene og med en frekvens på 112/min. Hunden peste ved undersøkelsen; med dette forbehold, var auskultasjon av hjerte og lunger uten anmerkning. Tilgjengelige lymfeknuter var symmetriske med normal størrelse og tekstur. Abdominal palpasjon var uten tydelige avvik. Hunden hadde ingen tegn til blødninger i hud, slimhinner eller ledd og rektaltemperaturen ble målt til 39,7 °C. En rektalundersøkelse ble ikke utført grunnet hundens temperament.
Diagnostiske undersøkelser
Hematologiske og biokjemiske analyser ble utført på henholdsvis IDEXX ProCyte og IDEXX Catalyst One (Tabell 1, Kasus IV, Dag 0), signifikante avvik inkluderte en moderat til markert trombocytopeni og en moderat økning i CRP. Det ble også påvist en markert lymfopeni og en svært mild ikke-regenerativ anemi.
Morfologisk undersøkelse av blodutstryk ble utført av klinisk patolog med funn av moderat til markert trombocytopeni, mild venstreforskyvning av nøytrofile granulocytter, markert lymfopeni og mulig svært mild anemi. I flere nøytrofile granulocytter var det basofile legemer forenlig med morulaer (Figur 2) og høyst suspekt med henblikk på infeksjon med A. phagocytophilum.
Det ble også utført en hurtigtest for vektorbårne infeksjoner (IDEXX Snap 4Dx Plus) som var negativ. I kateterurin ble det målt spesifikk vekt, samt utført en kjemisk analyse med urinstiks (IDEXX VetUA). Urinen hadde en spesifikk vekt på 1,044, og urinstiks viste utslag på protein (0,3 g/L, 1+) og blod (250 erytrocytter/µL, 4+). En PCR-undersøkelse for Anaplasma spp. utført på EDTA-stabilisert fullblod ved eksternt laboratorium (IDEXX Laboratories) var positiv.
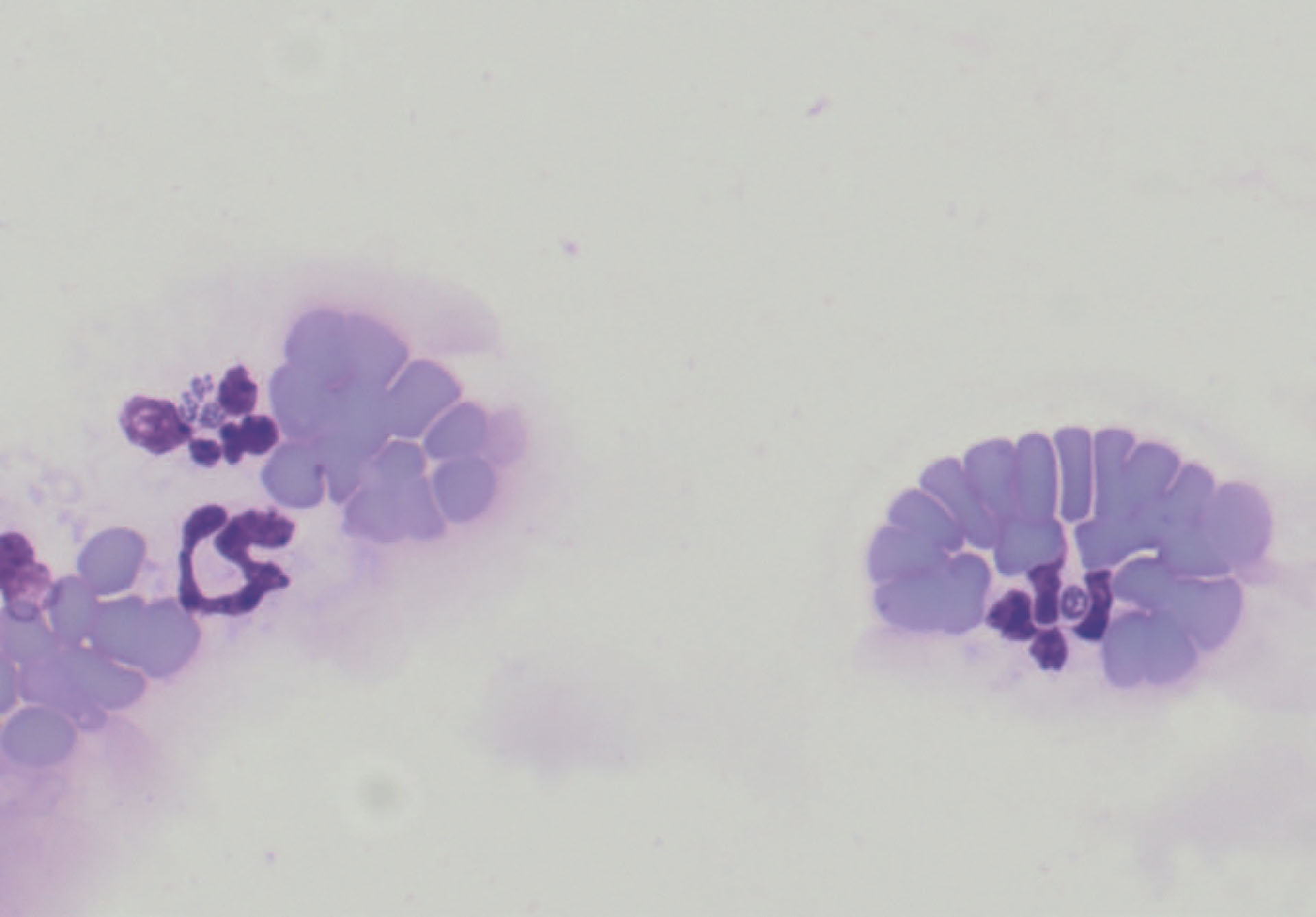
Figur 2. To ikke-intakte nøytrofile granulocytter i tungen av blodutstryket som inneholder morulaer. Erfaringsmessig er det ofte relativt lett å oppdage morulaer i denne delen av utstryket, men det er det såkalte monolaget av blodutstryket som benyttes til morfologisk vurdering. Farget med hurtigfarging (Hemacolor, Sigma-Aldrich). 40x objektiv.
Foto: Bente Kristin Sævik
Diagnose og behandling
Hunden ble behandlet med paracetamol (Paracet, KaroPharma) 10 mg/kg bid po i tre dager og maropitant (Vominil, VetVivaRichter) 1 mg/kg sc som en engangsbehandling på klinikken. Hunden ble ikke hospitalisert grunnet kort sykdomsforløp og relativt god allmenntilstand ved klinisk undersøkelse.
Kliniske og diagnostiske funn var forenlige med granulocytær anaplasmose. Behandling med doksysyklin (Ronaxan vet. Boehringer Ingelheim) 7,3 mg/kg bid po i 14 dager ble igangsatt og hunden ble sendt hjem. Ved telefonkonsultasjon dagen etter var hunden betydelig bedre, hadde begynt å spise og var afebril med en rektaltemperatur på 38,2 °C.
Oppfølging
Hunden kom til kontroll tolv dager etter innledende besøk. Eier opplevde da hunden som helt frisk igjen. Det var ingen avvik ved klinisk undersøkelse og nye hematologiske og biokjemiske analyser viste at blodplater og CRP nå var innenfor sine respektive referanseintervaller. Det forelå en mild retikulocytose (Tabell 1, Kasus IV, Dag 12). Det ble også utført en ny morfologisk undersøkelse som verifiserte telletallene, samt påviste en mild polykromasi. Morulaer ble ikke identifisert. Responsen på behandlingen med doksysyklin ble vurdert som svært god, og behandlingen ble anbefalt fullført.
Diskusjon
A. phagocytophilum tilhører familien Anaplasmataceae i ordenen Rickettsiales. I 2001 ble Ehrlichia equi, E. phagocytophila og agenset som forårsaker HGA (human granulocytær anaplasmose) tidligere HGE (human granulocytær ehrlichiose) (1,2,9) reklassifisert til A. phagocytophilum. Bakterien infiserer myeloide celler via endocytose, fortrinnsvis nøytrofile granulocytter, sjeldnere eosinofile granulocytter, ved primært å binde seg til overflateliganden P-selektin glykoprotein-1 (9-11). I vertscellen dannes intracytoplasmatiske inklusjoner på 1,5 – 2,5 µm, kalt morulaer (1,2,9). A. phagocytophilum frigjøres fra vertscellen ved hjelp av cytolyse, som fremmer infeksjon av flere celler og multiple organer (9,12).
Anaplasmose er en zoonose, og infiserte dyr kan være et viktig reservoar og kilde til infeksjon av vektorer. Selv om kjæledyr lever i tett kontakt med mennesker, er kjæledyr en mindre sannsynlig kilde til infeksjon hos mennesker. Dette er blant annet basert på funn i studier av seroprevalens hos mennesker med seropositive kjæledyr og mennesker uten kjæledyr (1,2). Bakteriemifasen hos hund er kort, noe som sannsynligvis begrenser hundens betydning som smittekilde (2). Ville karnivorer og gnagere er en mer sannsynlig kilde til overføring av flåttbårne sykdommer mellom mennesker og dyr (1,4,13). Det er imidlertid sett en korrelasjon mellom antall seropositive hunder og tilfeller av anaplasmose registrert humant. Antallet seropositive hunder i et gitt område kan gi en indikasjon om risikoen for human smitte (14).
Human anaplasmose har hatt økende forekomst i USA, Europa og Asia siden tidlig på 90-tallet (2) og er beskrevet sporadisk i Norge med totalt ni tilfeller rapportert frem til 2018 (8). At det er såpass få rapporterte tilfeller kan skyldes at de kliniske symptomene hos mennesker er lite spesifikke og milde.
Smitteoverføring uten vektor er beskrevet etter direkte kontakt med blod fra infiserte dyr eller mennesker, som blodtransfusjon (2,15). Ved transfusjon hos hund anbefales det at donorer av blod undersøkes for infeksjon med A. phagocytophilum ved serologi og PCR-undersøkelse (16). Prevalensen av seropositive hunder varierer mellom ulike land og regioner: 17 % i Sverige, 5,3 % i Finland, 50 % i Portugal og Italia, 50 % i Tyskland, 11,5 % i Spania og 46,1 % i Øst-Europa (1,12). Det er rapportert at 20/87 serumprøver (23 %) fra hunder i Aust-Agder var positive (17), men forekomsten vil også kunne variere med tidspunktet for studien.
Flåttbårne sykdommer angis å øke i utbredelse, sannsynlig grunnet global oppvarming og økende reiseaktivitet med kjæledyr (15,18). Dette kan føre til at flåttbårne sykdommer som ikke forekommer i Norge, diagnostiseres hos hunder etter reise. Agens fra hunder smittet i utlandet kan også overføres til vektorer her hjemme og dersom visse forutsetninger er oppfylt, bidra til at sykdommene etablerer seg i Norge. Økende utetemperatur vil kunne føre til at flåttpopulasjonen i Norge endres, blant annet ved etablering av nye arter som Rhipicephalus sanguineus (19).
Hundene i denne kasusserien hørte hjemme og oppholdt seg primært på Østlandet, og var mest sannsynlig smittet lokalt da ingen nylig hadde vært utenlands. Infeksjonstidspunktene gjenspeiler tidsperioden med aktiv flåttpopulasjon i det aktuelle området (9). I. ricinus er aktiv fra temperaturer rundt 6 °C (15) og utetemperaturen vil i stor grad påvirke hvor tidlig sesongen starter på våren og hvor lenge den varer utover høsten og vinteren. Kasus III ble syk så sent på året som i november. For å redusere risiko for infeksjon anbefales profylakse mot flått, samt rask fjerning av flått som har festet seg på hunden (2,4,15,19). Repellerende midler, syntetiske pyretroider, permetrin og deltametrin bør vurderes i områder med høy forekomst av A. phagocytophilum og andre flåttbårne agens (19). Basert på informasjon gitt av eier, hadde alle pasientene i denne kasusserien fått profylakse mot flått. Det finnes i dag ingen vaksine mot anaplasmose (4,15). Hvorvidt eier har observert flått på hunden vil variere (9,12), og var kun tilfelle med Kasus I. Dette understreker at flåttbårne sykdommer ikke kan utelukkes basert på fravær av denne observasjonen.
A. phagocytophilum angis å overføres fra flåtten til vertsdyret innen 24 til 48 timer, og bakteriemi oppstår fire til syv dager etter naturlig infeksjon (1,19). Bakterien nedregulerer funksjonene til nøytrofile granulocytter og påvirker motilitet, fagocytose, endoteladheranse, transmigrasjon og apoptose. Dette fører til at bakterien kan overleve og danne morulaer i celler som vanligvis har en kort levetid på ti til tolv timer (2).
Det er ikke beskrevet noen klar rase-, kjønns- eller aldersdisposisjon. Risikoen for smitte vil variere med årstid. Hunder som er mye ute i skog og mark vil kunne ha en større sannsynlighet for smitte enn hunder som oppholder seg primært i urbane strøk (2,15,18). I en belgisk studie ble det imidlertid påvist en høy forekomst av flått også i hager (44,3 %), spesielt i rurale områder (20). Eldre hunder er oftere seropositive enn yngre, sannsynlig grunnet økt risiko for eksponering over tid (15). I noen studier er retrievere overrepresentert. Dette gjenspeiler trolig at disse hundene oftere oppholder seg i eksponerte områder, heller enn en reell rasedisposisjon (11). Hundene i denne kasusserien var av fire ulike raser (strihåret vorstehhund, strihåret dachshund, dvergpuddel og tibetansk spaniel) med varierende alder, to kastrerte tisper og to intakte hannhunder.
Sykdom oppstår som oftest etter en til to ukers inkubasjonstid og de vanligste beskrevne kliniske tegnene er feber, slapphet, redusert appetitt, vekttap, samt muskel- og skjelett-smerter (1-4,10,11,13,18,19,21). Feberen kan undulere og toppen er angitt å sammenfalle med høyde-punktet for bakteriemi og sirkulasjon av morulaer (1-3,10,11). Lymfade-nomegali og splenomegali er også beskrevet, sannsynlig grunnet reaktiv lymfoid hyperplasi (1,2,4,9). Andre kliniske tegn som gastrointestinale tegn (diaré, kvalme, oppkast og buksmerter), polyuri, polydipsi, respiratoriske tegn, bleke slimhinner, blødningstilstander, uveitt, skleral karinjeksjon, polymyositt, effusjoner i ledd, hudlesjoner og nevrologiske tegn er også beskrevet (1-4,10,11).
Anaplasmose hos hund er regnet som en akutt sykdom med varighet på en til 14 dager, men det er beskrevet sykdomsforløp med opp til to måneders varighet (1). Alle de fire hundene i denne kasusserien ble undersøkt etter kort tids sykdom med milde til moderate og lite spesifikke sykdomstegn i form av redusert appetitt, letargi og feber. Kasus II og III hadde også smerter ved bukpalpasjon, Kasus II hadde i tillegg smerter fra leddene og bilateral uveitt. Kasus I hadde hatt mørkere avføring enn normalt, kun observert av eier, som kan ha vært sekundært til blødning i mage-tarmkanalen. Kasus I hadde i tillegg en mild forstørrelse av krøslymfeknuter og en mild splenomegali, påvist ved ultralydundersøkelse.
Kliniske tegn ved anaplasmose hos hund varierer fra milde til akutte og alvorlige, men milde kliniske tegn er beskrevet som vanlig (10). Uoverensstemmelse mellom antallet seropositive og syke hunder i epizootiske områder, tyder på at tilstanden er selvbegrensende i mange tilfeller (1-3,22). Subklinisk sykdom er beskrevet hos opp til 60 % av seropositive hunder (13) og granulocytær anaplasmose hos hund kan derfor være underdiagnostisert.
Kronisk eller persisterende infeksjon hos naturlig infiserte hunder er et kontroversielt tema (1-3,11), men er beskrevet hos eksperimentelt inokulerte hunder (12,15). Reinfeksjon er beskrevet humant (15) og er sannsynlig også forekommende hos hund (11).
Koinfeksjoner med andre vektorbårne agens som B. burgdorferi, E. canis og Babesia canis er vanlig i epizootiske områder. Dette fører til mer alvorlige og komplekse kliniske tegn enn ved infeksjon med A. phagocytophilum alene (1,2,4,10,11). Redusert nøytrofilfunksjon vil også kunne predisponere for sekundære, opportunistiske infeksjoner som kan komplisere det kliniske sykdomsbildet (2,4,9).
Vanlige beskrevne hematologiske endringer ved granulocytær anaplasmose hos hund inkluderer trombocytopeni, anemi, leukopeni og lymfopeni, men varierende leukocyttall er beskrevet (1,2,10,12, 15,21,23). Cytopenier oppstår sannsynligvis grunnet myelosuppresjon, dannelse av autoantistoffer, infeksjon av forløperceller og forbruk. Trombocytopeni er beskrevet hos 16,7-95 % av naturlig infiserte hunder og anses, etter påvisning av morulaer, som det mest typiske hematologiske avviket (1-3,10-13,21,23). I denne kasusserien, ble trombocytopeni påvist hos alle hundene og vurdert som markert hos Kasus I og III, og moderat til markert hos de to andre.
Trombocytopenien ved A. phagocytophilum infeksjon hos hund varierer fra mild til markert, med lavere platetall rapportert hos hunder som har koinfeksjon med B. burgdorferi (1,2,11). A. phagocytophilum kan infisere megakaryocyttlinjer, men angivelig uten å påvirke evnen til produksjon av blodplater (24). Trombocytopenien er derfor sannsynlig assosiert med den inflammatoriske prosessen, økt destruksjon og forbruk av blodplater, heller enn organismen i seg selv. Aktuelle årsaker er disseminert intravaskulær koagulasjon (DIC), sekvestrering i milt, immunologisk betinget platedestruksjon og/eller produksjon av inhibitoriske faktorer (1,2,9,10,12,23). Antistoffer bundet til plater er påvist hos noen individer (12). Det laveste platetallet korrelerer med bakteriemifasen, og platetallet normaliseres som oftest noen dager etter at denne fasen er avsluttet (9,23). Anemi er et mindre hyppig funn, og i sjeldne tilfeller er det rapportert immunmediert hemolytisk anemi (1-3,9,11,12,15). Bortsett fra Kasus IV som hadde en svært mild anemi, var de andre kasusene ikke anemiske, hverken ved innledende undersøkelse eller ved kontrollbesøk. Ved kontroll forelå det ikke lenger en anemi, men kun en mild retikulocytose hos Kasus IV.
Påvisning av morulaer i nøytrofile granulocytter, sjeldnere i eosinofile granulocytter, ved morfologisk undersøkelse av blodutstryk er forenlig med infeksjon med A. phagocytophilum (1-4,10). Morulaer ble observert i blodutstryk hos alle fire kasus i denne serien. Disse er synlig som basofile inklusjoner i bakteriemifasen (fire til 14 dager etter infeksjon) og kan påvises i fire til åtte dager (1,2,13,15). Andelen nøytrofile granulocytter som inneholder morulaer varierer fra 1 til 34 %, og en høyere prosentandel infiserte celler er angitt å være assosiert med mer alvorlige kliniske tegn (1). A. phagocytophilum morula kan ikke skilles fra E. ewingii morula, og i epizootiske områder vil andre diagnostiske undersøkelser som PCR være nødvendig for å skille disse (1-3,15). Fravær av morulaer i blodutstryk utelukker ikke infeksjon med A. phagocytophilum (13), da dette er beskrevet i opptil 60 % av kliniske tilfeller (15).
Endringer i antallet og andelen leukocytter varierer. Det kan påvises både leukocytose, leukopeni, lymfocytose, eosinopeni, monocytose, nøytropeni og nøytrofili med eller uten venstreforskyvning, men lymfopeni er hyppigst beskrevet (1-3). Endringer i andelen leukocytter ble observert hos Kasus I som hadde en mild lymfopeni og en mild nøytropeni, og hos Kasus IV som hadde en markert lymfopeni. Tre av kasusene hadde imidlertid venstreforskyvning av de nøytrofile granulocyttene, forenlig med inflammasjon. Kasus III hadde nøytrofili ved kontrollbesøk, muligens relatert til stress.
Vanlige biokjemiske endringer rapportert er økte leverenzymer, hyperbilirubinemi, hypofosfatemi, hyperproteinemi, hyperglobulinemi og hypoalbuminemi (1,2,9,11,12, 19,23). Samtlige kasus hadde biokjemiske analyser uten klinisk signifikante avvik med unntak av moderat til markert forøket CRP. Konsentrasjonen av akuttfaseproteiner som CRP er ikke undersøkt i majoriteten av publiserte studier, men en økning vil være naturlig assosiert med en inflammasjon relatert til den systemiske bakterielle infeksjonen som foreligger.
Funn ved urinanalyser hos hund med granulocytær anaplasmose er mindre kjent enn de klinisk patologiske funnene i blod (1). Det er imidlertid beskrevet både isostenuri, proteinuri, glukosuri, bilirubinuri og hematuri (1,11,19,23). Det er en mulighet for at persisterende infeksjon med A. phagocytophilum kan føre til immunmediert glomerulonefritt, men de fleste infeksjoner hos hund antas å være akutte (1). Urinanalyser ble utført hos alle hundene i denne kasusserien, dels etter væskeinfusjon som høyst sannsynlig har påvirket urinens tetthet hos Kasus II og III. Kjemiske analyser viste utslag på blod uten synlig makroskopisk blodtilblanding. Hos Kasus II, III og IV kan dette være grunnet iatrogen blødning fra henholdsvis cystocentese og kateterisering, uansett ble ikke dette funnet verifisert mikroskopisk. Sett i lys av at Kasus II hadde en moderat til markert trombocytopeni, kunne urinanalyse med fordel vært utført på skålurin for å redusere risikoen for iatrogen blødning. Kasus I hadde også 3+ proteinuri. Protein/kreatinin ratio i urinen (UPC) ble ikke målt og urinundersøkelsen ble ikke gjentatt, noe som kunne ha blitt gjort når hunden var i remisjon. Vi kan derfor ikke utelukke en proteinuri relatert til infeksjonen eller at hunden allerede hadde en proteinuri. Proteinuri kan muligens også oppstå ved sykdomstilstander karakterisert av feber og systemisk inflammasjon (25).
Serologiske tester i diagnostiske laboratorier utføres som oftest ved hjelp av immunfluorescent antistoffteknikk (IFAT) eller ELISA (2,9,13,15). Det finnes også flere pasientnære tester til bruk i klinikken, oftest kvalitative eller semikvantitative (15). IgG antistoffer er først mulig å påvise cirka åtte dager etter infeksjon, og to til fem dager etter at morulaer er synlig i granulocytter (2,9,13,15). Dette kan føre til at en andel klinisk syke hunder ikke har høye nok antistofftitere til å kunne påvises med serologiske tester når de undersøkes (3). Det er angitt at fra 25-40 % er seronegative ved innledende presentasjon (3,10). Hundene i denne kasusserien fikk alle utført en pasientnær test med IDEXX Snap 4DX. Dette er en ELISA-basert test som binder til p44 proteinet i A. phagocytophilum (14,21). Denne testen har en rapportert sensitivitet på 94,1-99,1 % og en rapportert spesifisitet på 98,8-100 % (13,21). Kasus II hadde positiv hurtigtest for Anaplasma spp., mens Kasus I, III og IV hadde negative resultater. Kvantifisering av antistoffer mot A. phagocytophilum ble i tillegg utført hos Kasus II ved ELISA undersøkelse og var positiv (50,3 TU; RI: 0-8).
Mer enn firefolds økning i antistofftiter, målt i parprøver tatt med flere ukers mellomrom, vil vanligvis være forenlig med aktiv infeksjon. Antistoffer kan persistere i lengere tid etter gjennomgått infeksjon og økt antistofftiter på en enkelt prøve kan reflektere tidligere eksponering heller enn pågående infeksjon (2,15,19). En positiv serologisk test alene er ikke indikasjon for behandling med antibiotika (10). En innledende negativ kvalitativ test, vil også kunne gjentas etter to til fire uker og vil indikere nylig infeksjon om resultatet er positivt på den siste testen (15). Persisterende antistoffer etter A. phagocytophilum-infeksjon er beskrevet i opptil ett år, men det finnes lite informasjon om dette (15). En ny kvantitativ undersøkelse av antistoffer ble utført hos Kasus II etter åtte måneder og nivået hadde da sunket betraktelig og var innenfor referanseintervallet. Serologiske kryssreaksjoner med andre Anaplasma spp. som A. platys kan også forekomme (2,15,21).
PCR er en spesifikk og sensitiv undersøkelse for å diagnostisere akutt anaplasmose hos hund. Et positivt resultat er vanligvis forenlig med infeksjon (2,3,15). PCR-undersøkelse for A. phagocytophilum utføres primært på EDTA-stabilisert fullblod (15) og kan være positiv så tidlig som to dager etter infeksjon (12). PCR-undersøkelse av miltvev kan brukes ved mistanke om bærerstatus, spesielt hos ville dyr (1,4). Det er også beskrevet positivt PCR-resultat i aspirert materiale fra lymfeknuter (22).
Hos eksperimentelt infiserte hunder er det påvist positivt PCR-resultat seks til åtte dager før og tre dager etter påvisning av morulaer i blodutstryk (2). Kasus II, III og IV hadde positivt PCR-resultat for A. phagocytophilum på EDTA-stabilisert fullblod. PCR-undersøkelse ble ikke utført på blod fra Kasus I da kombinasjonen av kliniske tegn, påvisning av trombocytopeni og morulaer samme dag som hunden ble hospitalisert ble ansett som tilstrekkelig for å stille diagnosen granulocytær anaplasmose med stor sikkerhet.
PCR-undersøkelser for A. phagocytophilum kan være positive hos klinisk friske hunder og negative hos infiserte hunder, sistnevnte sannsynlig grunnet variasjon i antallet sirkulerende organismer (3,13). Det finnes ulike PCR-undersøkelser, blant annet basert på msp2 og 16S rRNA, der sistnevnte også kan gi et positivt resultat for andre Anaplasma spp. (2).
Et negativt PCR-resultat etter gjennomført behandling vil støtte at behandlingen har vært effektiv og at agens er eliminert (9,15). En ny PCR-undersøkelse ble utført på EDTA-stabilisert fullblod fra Kasus II tre uker etter behandlingsstart med doksysyklin, og denne var negativ.
Behandling av granulocytær anaplasmose hos hund med doksysyklin er angitt å være effektiv, ofte med god klinisk bedring innen 24-48 timer. En forsinket behandlingsrespons på opptil seks dager er også beskrevet (2,3,10,11,15,22). Dosering av doksysyklin tabletter angis fra 5-11 mg/kg bid eller 8-11 mg/kg sid, med behandlingslengde fra to til fire uker (2-4,9-12,15,22), mens det humant anbefales ti dager behandling (3). Hos valper er behandling med kloramfenikol angitt som et alternativ til doksysyklin (15). Alle pasientene i denne kausserien ble behandlet med doksysyklin (7,3-10 mg/kg bid po, avhengig av kroppsvekt og passende tablettstyrke), men med ulik behandlingslengde fra to til fire uker. Alle pasientene fikk i tillegg støttebehandling i form av krystalloid væske (med unntak av Kasus IV), antiemetika (maropitant) og antipyretika (paracetamol), grunnet redusert appetitt, letargi og pyreksi, i påvente av en etiologisk diagnose.
Det vil være mange aktuelle differensialdiagnoser for de vanligste kliniske tegnene ved granulocytær anaplasmose. Sykdommen bør derfor vurderes ved lite spesifikke kliniske tegn som feber, letargi, redusert appetitt, splenomegali og halthet og/eller laboratorieavvik som trombocytopeni, anemi, lymfopeni, økt CRP og hypoalbuminemi (9), også der flått ikke er observert på hunden (12). Nylig ble det også publisert en kasuistikk hvor en hund fikk indusert en klonal T-celle proliferasjon ved akutt anaplasmose, som ble feildiagnostisert som lymfom (26).
Prognosen anses generelt som god, med rask remisjon etter behandling med doksysyklin. Dødsfall er imidlertid beskrevet, oftest sekundært til komplikasjoner som immunmediert hemolytisk anemi, og/eller ved koinfeksjoner med andre agens, samt hos eldre dyr (1,3). De fire kasusene i denne serien viste alle rask klinisk bedring etter behandling med doksysyklin, samt en tydelig økning i platetallet og reduksjon i konsentrasjonen av CRP i kontrollblodprøve.
Konklusjon
Granulocyttær anaplasmose påvises hos hund i Norge. De kliniske tegnene er uspesifikke. Økt CRP og trombocytopeni er vanlig. Morfologisk undersøkelse av blodutstryk er viktig for å se etter plateklumper (pseudotrombo-cytopeni) og morulaer. Pasientnære hurtigtester for påvisning av antistoff kan ofte være negative, mens PCR-undersøkelse har høy sensitivitet i fasen med kliniske tegn.
Sammendrag
Artikkelen beskriver granulocytær anaplasmose hos hund basert på en kasusserie med fire kasus. Infeksjonen overføres via flått, oftest i slekten Ixodes. Granulocytær anaplasmose er regelmessig forekommende hos hunder i Norge, og kan også opptre hos hunder som får jevnlig profylaktisk behandling mot flått.
Hos hund ses ofte lite spesifikke kliniske tegn som redusert allmenntilstand, redusert matlyst, feber og muskel- og skjelettsmerter. Dette gjør at sykdommen kan feildiagnostiseres. Det vanligste hematologiske avviket er trombocytopeni, og morulaer kan påvises i nøytrofile granulocytter i den akutte sykdomsfasen. Økt CRP indikerer systemisk inflammasjon.
Hunder kan også ha svært milde kliniske tegn og selvbegrensende sykdom. Dette fører til at mange hunder kan ha høye antistoffnivåer fordi de har gjennomgått subklinisk infeksjon tidligere. På den annen side kan pasientnære antistofftester ofte være negative tidlig i sykdomsforløpet, mens PCR-undersøkelse har en høy sensitivitet for påvisning av infeksjon i denne fasen. Behandling med doksysyklin gir generelt en god og rask respons, og prognosen er ansett som god.
Summary
Canine granulocytic anaplasmosis.
A case series with four cases.
This article describes granulocytic anaplasmosis in dogs through a case series with four cases. The infection is transmitted by ticks, most often in the genus Ixodes. Granulocytic anaplasmosis is common in dogs in Norway and can occur despite regular prophylactic treatment against ticks.
In dogs, non-specific clinical signs, such as reduced general condition, decreased appetite, fever, and musculoskeletal pain, are common, which can easily lead to misdiagnosis. The most common haematological abnormality is thrombocytopenia. Morulae can be detected in neutrophil granulocytes in the acute phase of the disease. Increased CRP indicates systemic inflammation.
In dogs, the disease may be mild or self-limiting, resulting in high antibody levels from previous subclinical infections. In contrast, point-of-care antibody tests may often be negative early in the course of disease, whereas PCR has high sensitivity for detecting infection during this phase. Treatment with doxycycline generally leads to a favourable and rapid response, and the prognosis is good.
Referanser
Khatat SEH, Daminet S, Duchateau L, Elhachimi L, Kachani M, Sahibi H. Epidemiological and clinicopathological features of Anaplasma phagocytophilum infection in dogs: a systematic review. Front Vet Sci 2021;8:686644.
Carrade DD, Foley JE, Borjesson DL, Sykes JE. Canine granulocytic anaplasmosis: a review. J Vet Intern Med 2009;23:1129-41.
Eberts MD, Diniz PPVP, Beall MJ, Stillman BA, Chandrashekar R, Breitschwerdt EB. Typical and atypical manifestations of Anaplasma phagocytophilum infection in dogs. J Am Anim Hosp Assoc 2011;47:e86-94.
Atif FA, Mehnaz S, Qamar MF, Roheen T, Sajid MS, Ehtisham-ul-Haque S et al. Epidemiology, diagnosis, and control of canine infectious cyclic thrombocytopenia and granulocytic anaplasmosis: emerging diseases of veterinary and public health significance. Vet Sci 2021;8:312.
Andreassen TH, Havang I, Ulsrud Myren IK. Forekomst av Borrelia burgdorferi sensu lato og Anaplasma phagocytophilum i Ixodes ricinus fra to områder i Viken fylke. Ås 2021. Fordypningsoppgave - Norges miljø- og biovitenskapelige universitet.
Kjelland V, Paulsen KM, Rollum R, Jenkins A, Stuen S, Soleng A et al. Tick-borne encephalitis virus, Borrelia burgdorferi sensu lato, Borrelia miyamotoi, Anaplasma phagocytophilum and Candidatus Neoeherlichia mikurensis in Ixodes ricinus ticks collected from recreational islands in southern Norway. Ticks Tick Borne Dis 2018; 9: 1098-102.
Henningsson AJ, Hvidsten D, Kristiansen BE, Matussek A, Stuen S, Jenkins A. Detection of Anaplasma phagocytophilum in Ixodes ricinus ticks from Norway using a realtime PCR assay targeting the Anaplasma citrate synthase gene gltA. BMC Microbiol 2015;15:153.
Folkehelseinstituttet. Anaplasmose: håndbok for helsepersonell. Sist endret 10.03.2023. https://www.fhi.no/sm/smittevernhandboka/sykdommer-a-a/anaplasmose/ (27.11.2025).
Kohn B, Galke D, Beelitz P, Pfister K. Clinical features of canine granulocytic anaplasmosis in 18 naturally infected dogs. J Vet Intern Med 2008;22:1289-95.
Granick JL, Armstrong PJ, Bender JB. Anaplasma phagocytophilum infection in dogs: 34 cases (2000-2007). J Am Vet Med Assoc 2009;234:1559-65.
Mazepa AW, Kidd LB, Young KM, Trepanier LA. Clinical presentation of 26 Anaplasma phagocytophilum-seropositive dogs residing in an endemic area. J Am Anim Hosp Assoc 2010;46:405-12.
Chirek A, Silaghi C, Pfister K, Kohn B. Granulocytic anaplasmosis in 63 dogs: clinical signs, laboratory results, therapy and course of disease. J Small Anim Pract 2018;59:112-20.
Duncan K, Burton KW. Diagnosing and managing Anaplasma infection in dogs. Today’s Vet Pract 2024;14(3):28-32.
Braff JC, Arguello-Marin A, Hanscom J, Saucier J, Beall MJ, Qurollo BA et al. Evaluation of Anaplasma spp. seroprevalence in dogs and association with incidence of human anaplasmosis. Vet Parasitol Reg Stud Reports 2023;45:100923.
Sainz Á, Roura X, Miró G, Estrada-Peña A, Kohn B, Harrus S et al. Guideline for veterinary practitioners on canine ehrlichiosis and anaplasmosis in Europe. Parasit Vectors 2015;8:75.
Wardrop KJ, Birkenheuer A, Blais MC, Callan MB, Kohn B, Lappin MR et al. Update on canine and feline blood donor screening for blood-borne pathogens. J Vet Intern Med 2016;30:15-35.
Åkerstedt J, Blakstad E, Artursson K. Seroprevalens av Borrelia burgdorferi sensu lato og Ehrlichia sp. hos hund fra et kystområde i Aust-Agder. Nor Vet Tidsskr 1996;108:537-43.
Facile V, Sabetti MC, Balboni A, Urbani L, Tirolo A, Magliocca M et al. Detection of Anaplasma spp. and Ehrlichia spp. in dogs from a veterinary teaching hospital in Italy: a retrospective study 2012-2020. Vet Res Commun 2024;48:1727-40.
Silvestrini P, Lloyd-Bradley B, Glanemann B, Barker EN, Badham H, Tappin S et al. Clinical presentation, diagnostic investigations, treatment protocols and outcomes of dogs diagnosed with tick-borne diseases living in the United Kingdom: 76 cases (2005-2019). J Small Anim Pract 2023;64:392-400.
Robert K, Van Gestel M, Lathouwers M, Fonville M, Sprong H, Matthysen E et al. Abundance of ticks and tick-borne pathogens in domestic gardens in Belgium, 2020-2022: a citizen science approach. BMC Public Health 2025;25:2031.
Chandrashekar R, Mainville CA, Beall MJ, O`Connor T, Eberts MD, Alleman AR et al. Performance of a commercially available in-clinic ELISA for the detection of antibodies against Anaplasma phagocytophilum, Ehrlichia canis, and Borrelia burgdorferi and Dirofilaria immitis antigen in dogs. Am J Vet Res 2010;71:1443-50.
Yancey CB, Diniz PPVP, Breitschwerdt EB, Hegarty BC, Wiesen C, Qurollo BA. Doxycycline treatment efficacy in dogs with naturally occurring Anaplasma phagocytophilum infection. J Small Anim Pract 2018;59:286-93.
Ravnik U, Tozon N, Smrdel KS, Zupanc TA. Anaplasmosis in dogs: the relation of haematological, biochemical and clinical alterations to antibody titre and PCR confirmed infection. Vet Microbiol 2011;149:172-6.
Granick JL, Reneer DV, Carlyon JA, Borjesson DL. Anaplasma phagocytophilum infects cells of the megakaryocytic lineage through sialylated ligands but fails to alter platelet production. J Med Microbiol 2008;57:416-23.
Ruane E, Rodgers MMA, Hare CHZ, McCallum KE, Williams TL. Investigation of association between serum C-reactive protein concentrations and proteinuria in dogs. J Small Anim Pract 2025. https://doi.org/10.1111/jsap.70040
Teichner SR, Powell LL, Mazepa AS. Clonal T cell proliferation induced by acute anaplasmosis in a dog. J Vet Intern Med 2025;39:e70233.