Aktuelle sykdomsutbrudd og diagnoser
Veterinærinstituttet
Pharmaq Analytiq
Aktuelle diagnoser, «nye» sykdommer og spesielle tilfeller har i mange år blitt presentert under vignetten «Aktuelle sykdomsutbrudd og diagnoser fra Veterinærinstituttet, Mattilsynet og NMBU Veterinærhøgskolen». Redaksjonen er av den oppfatning at dette er nyttig og lett tilgjengelig informasjon som bidrar til å opprettholde medlemmenes kunnskap om utviklingen innen diagnostikk og overvåkning av sykdomssituasjonen i Norge. Vi har inntrykk av at denne spalten oppfattes som nyttig og interessant informasjon som gjerne leses av tidsskriftets lesere.
Det er i det alt vesentlige Veterinærinstituttets diagnostiske laboratorier, Mattilsynet og NMBU Veterinærhøgskolen som har bidratt med nytt om sykdom og helse hos produksjonsdyr, fisk, vilt og familiedyr. I tillegg har veterinærer i felten bidratt med selve forutsetningen for at kasuistikkene kan beskrives; innsendelse av materiale, informasjon om besetning/anlegg, anamnese og behandling. I de senere år har det dukket opp flere aktører, særlig innen fiskehelse, som tilbyr diagnostiske tjenester i konkurranse med de offentlige og veletablerte laboratorier. Det er grunn til å anta at private aktører vil ta over en stadig større del av denne diagnostiske virksomheten. Redaksjonen i NVT mener at mange av de funn/diagnoser som gjøres ved disse laboratorier vil være av interesse for NVTs lesere, og vi inviterer private laboratorier til å sende inn meddelelser om interessante kasus på lik linje med det etablerte offentlige laboratorier gjør i dag. Innlegg fra private aktører vil bli gjenstand for samme redaksjonelle behandling som dagens innlegg.
Stikkord er korte og konsise innlegg som er anonymisert, og med stedsangivelse på fylkesnivå. Lengden på innlegget bør normalt ikke overstige 500 ord, og det er ønskelig med illustrasjoner/bilde(r). Både vanlige og spesielle diagnoser/sykdomsutbrudd er ønsket, men diagnosen må ha en viss aktualitet. Sykdomstilfellet/utbruddet kan beskrives kort med hensyn på omfang, klinikk og patologi, grunnlag for diagnosen, forløp, utfall, tiltak samt forvaltningsmessige forhold. Detaljerte beskrivelser av makroskopiske og mikroskopiske funn bør unngås, likeså mikrobiologiske detaljer. Det er aktuelt med henvisninger til eventuelle lignende utbrudd fra litteraturen.
Redaksjonskomiteen
Nyresvulst hos atlantisk laks
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet mottok prøver tatt ut høsten 2019 fra et matfiskanlegg med laks (Salmo salar) i Nord-Norge i forbindelse med rutinemessig prøveuttak for histologisk vurdering av gjellestatus. Under obduksjon av en dødfisk på anlegget observerte innsender fisk, 1 kg, med tydelig avgrenset utvekst lokalisert i kaudale del av nyre (figur 1), og tok ut (kun) nyreprøver for histologi fra denne fisken.
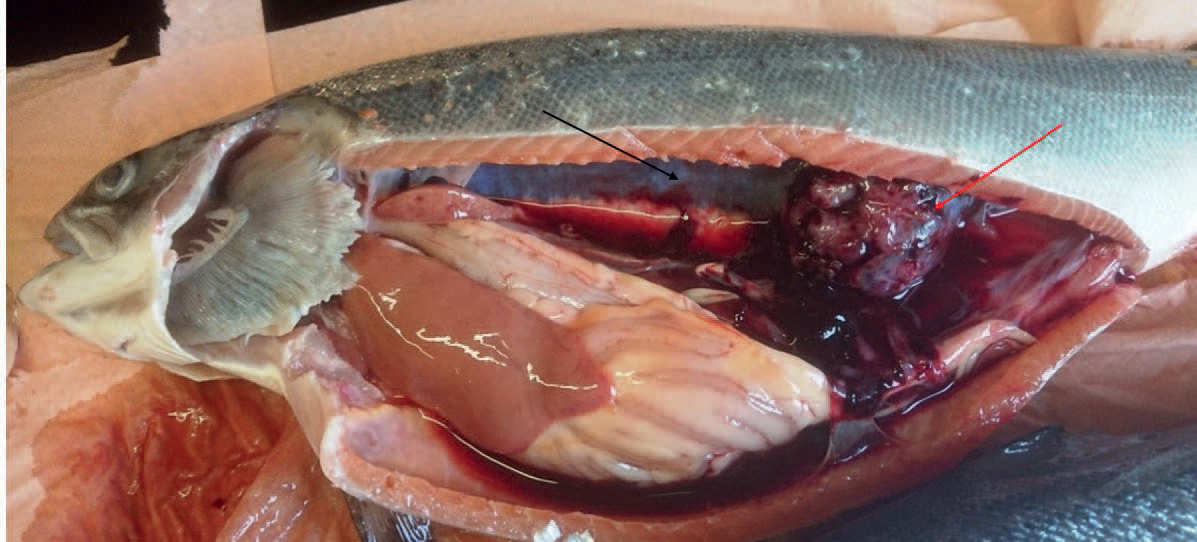
Figur 1: Makroskopisk bilde av utvekst (rød pil) i nyreområdet (sort pil). Bilde: Kristoffer Vale Nielsen
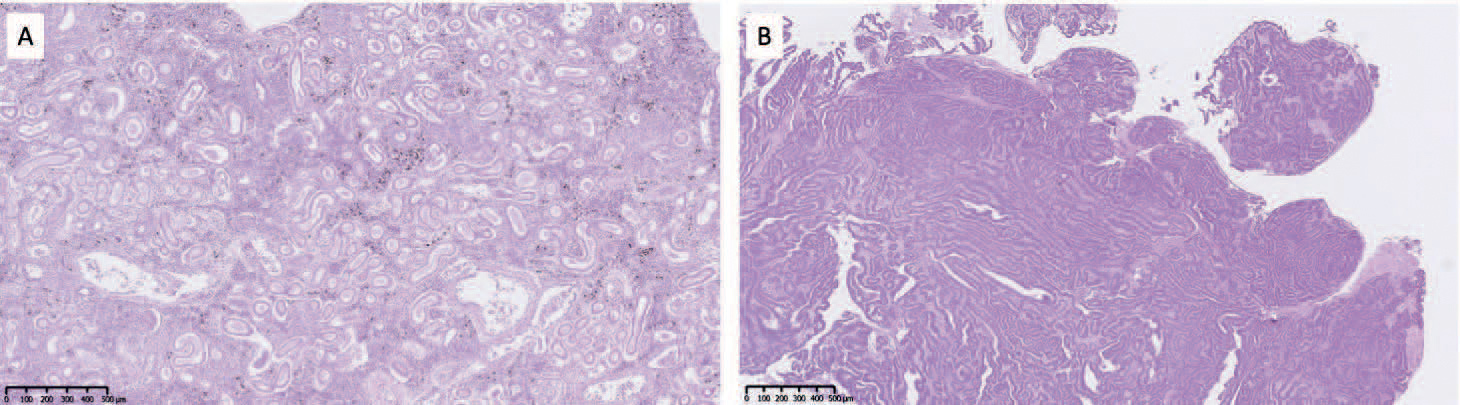
Figur 2: Histologibilder (HE-farging) av nyre (A) og svulst i nyreområdet (B). Målestokk 500 mm. Bilde: Synne Grønbech
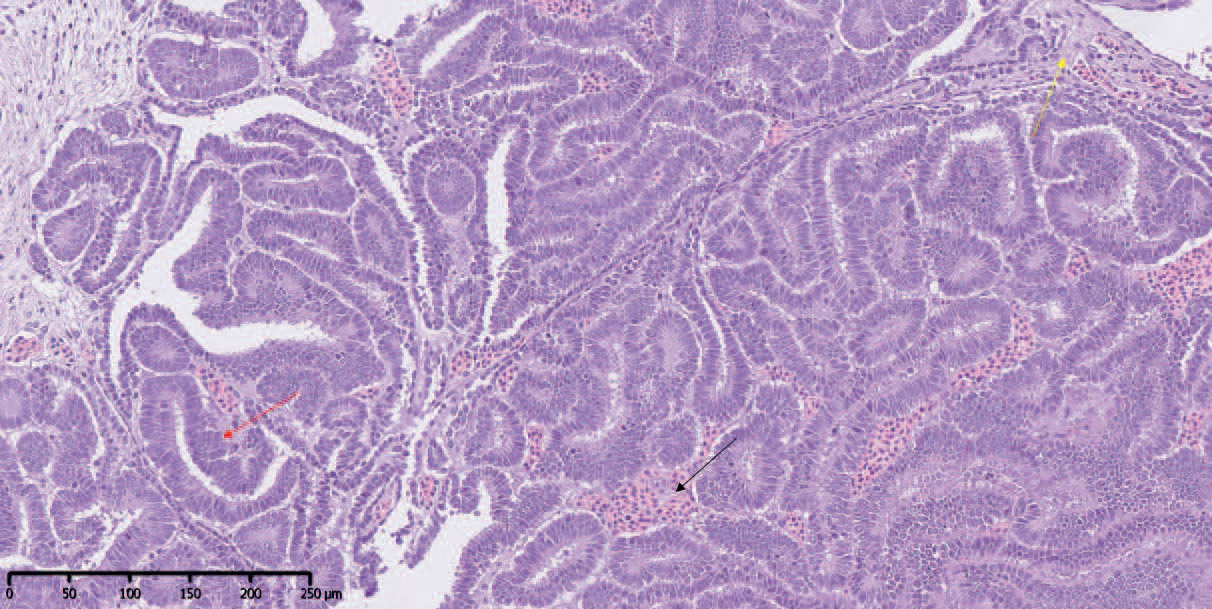
Figur 3: Histologibilde (HE-farging) av nyresvulst. Tubulære strukturer med flerradet epitel (rød pil). Blodansamlinger mellom strukturer (sort pil). Bindevevsavgrensinger (gul pil). Målestokk 250 mm. Bilde: Synne Grønbech
Prøvene ble snittet og rutinemessig farget med hematoksylin-eosin (HE) (figur 2). Histologisk undersøkelse viste kjertellignende forandringer i prøve tatt fra utvekst av det som morfologisk ligner på tubulære strukturer med epiteldysplasi (fremstår med flerradet epitel) med interne bindevevsavgrensninger som stedvis er blodfylte (figur 3). Overgang til normalt nyrevev kunne ikke sees i snittet. I separat nyreprøve tatt i mer kraniale deler av nyre ble det foruten post-mortelle forandringer observert noe forekomst av fibrose i interstitium mellom/rundt tubuli og eosinofilt (lyserosa) konkrementaktig materiale i lumen av en del tubuli. Funn fra utvekst peker på nydannelse, men det er vanskelig å si hvorvidt denne er av godartet eller ondartet karakter. Det er usikkert om tumoren utgår fra nyrevevet og om det er invasiv vekst i nyret, om det er lokal ekspansiv vekst fra nærliggende vev (for eksempel urinblære eller svømmeblære) eller om det skyldes spredning/metastase fra et annet organ. Fargemetode for å lete etter slimceller som indikasjon på spredning fra tarmvev, periodic-acid-schiff (PAS), ble gjennomført uten positivt funn. Basert på histologiske funn av utveksten ble det stilt en diagnose om tumor (svulst), mulig forenlig med papillært adenom (godartet tumor), men det var vanskelig å konkludere om tumoren var godartet eller ondartet.
Det er relativt få rapporterte forekomster av nyresvulster hos fisk i litteraturen. De fleste primære/spontane nydannelser (neoplasier) i nyre består av enkelttilfeller. De mest vanlige typene hos fisk er nefroblastomer, former av adenomer/adenokarsinomer og lymfomer/leukemi. I sjeldne tilfeller har det vært antydning til genetisk predisponering for spesifikke neoplasier i nyre hos noen populasjoner av enkelte marine arter, med miljøbetinget eller ukjent infeksiøs årsak fungerende som promotor til karsinogenese (1). I tråd med litteraturen (1, 2) diagnostiserer vi sporadiske tilfeller av nefroblastomer, særlig hos regnbueørret.
Selv om det vanskelig å konkludere om svulsten i dette tilfellet er godartet eller ondartet basert på histologisk undersøkelse, er det nærliggende å tenke at en svulst av slik størrelse påvirker funksjonen av vev/strukturer i området som for eksempel urinleder. En økt forekomst av tilfeller i populasjonen er uønsket.
Kilde:
Lombardini ED, Hard GC, Harshbarger JC. Neoplasms of the urinary tract in fish. Vet Pathol 2014; 51: 1000-12.
Martineau D, Ferguson HW. Neoplasia. I: Ferguson HW, ed. Systemic pathology of fish: a text and atlas of normal tissues in teleosts and their responses in disease. 2nd ed. London: Scotian Press, 2006: 331-5.
Hjertecyster hos atlantisk laks (Salmo salar)
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet mottok vinteren 2020 prøvemateriale fra et matfisk-anlegg for atlantisk laks i Nord-Norge. Anlegget hadde forøket dødelighet i en merd hvor mesteparten av dødfisken hadde sår. Ved obduksjon i felt var det hovedsakelig få funn i indre organer, med unntak av enkeltindivider med tegn til sirkulasjonssvikt. Det ble tatt ut standard organpakke, i tillegg til prøver av sår fra tre svimere til histologisk undersøkelse. Laksene var sjøsatt tidlig sommer året før, hadde kroppsvekt på cirka 2,8 kg og var vaksinerte. Sjøtemperatur var cirka 3,3 grader.
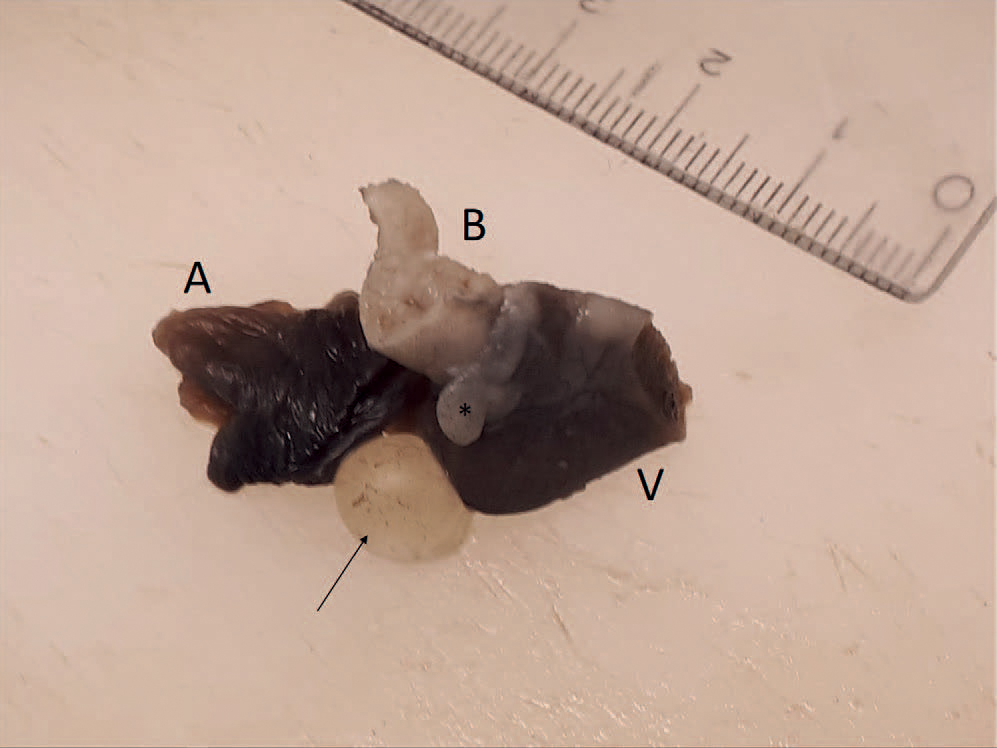
Figur 1. Laksehjerte med utvendig stor (pil) og mindre (*) cyste. Atrium (A), ventrikkel (V), bulbus arteriosus (B). Bilde: Toni Erkinharju, Veterinærinstituttet.
Hjertet fra ett av disse individene hadde utvendige makroskopiske forandringer. På øvre del av ventrikkelen, nær atrium, ble det observert en væskefylt cyste på cirka 1 cm i diameter (Figur 1). Ved punktering av denne kom det ut tilnærmet klar væske som det ble laget tre utstryk av på objektglass. Første utstryk ble fiksert med bruk av åpen flamme. Det andre ble fiksert i metanol, og det tredje var uten fiksering. Utstrykene ble så cytologisk farget med May-Grünwald-Giemsa (MGG). Ved mikroskopering ble det observert rikelig med erytrocytter og moderat med leukocytter, hvorav flere var klumpet sammen i større aggregater. Innimellom blodcellene ble det funnet svært sparsomt med lange, filamentøse og korte til kokkoide stavbakterier liggende enkeltvis eller flere tettpakket i større mikrokolonier (Figur 2). Lignende bakterier ble også funnet histologisk i rikelig mengde i dype hudsår hos samme individ.
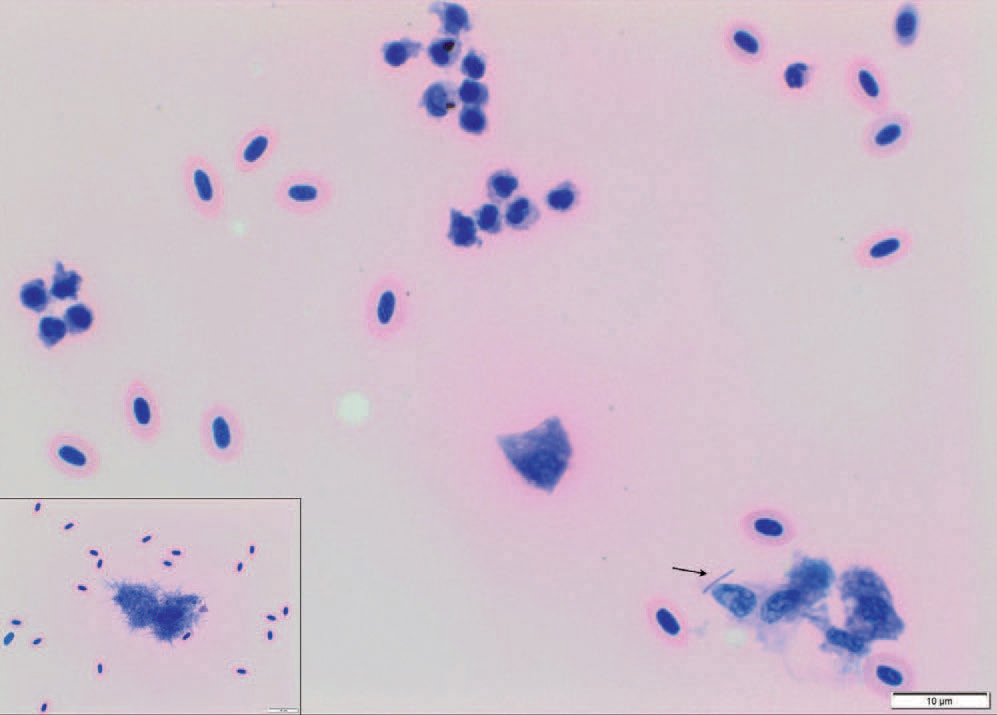
Figur 2. Utstryk fra hjertecyste, farget med MGG. Blant erytrocytter og leukocytter sees sparsomt med stavbakterier liggende fritt enkeltvis (pil) eller tettpakket i større klumper (innfelt). Målestokk 10 mm. Bilde: Toni Erkinharju, Veterinærinstituttet.
Ved histologisk undersøkelse av hjertet ble rester av cysteveggen beskrevet som lange, avsnørende, slintreaktige remser av epikardlaget på ventrikkelen. Deler av vevet, særlig ved festepunktet på epikard, var sparsomt infiltrert av leukocytter, eosinofile granulære celler (EGC) og celler som minner om atypiske plasmaceller (Mott celler) (Figur 3A-C). Fokalt på en av atrioventrikulær (AV)-klaffene ble det også funnet en cyste fylt med et lyst eosinofilt væskelignende innhold med enkelte hvite og røde blodceller i randsonen av innholdet (Figur 3D-E). Øvrige funn i hjertet var moderat epikarditt, sparsom endokarditt, multifokale mikrotrombedannelser av varierende størrelse, rikelig infiltrasjon av EGC ved overgang mellom bulbus arteriosus og ventrikkel, tegn til forøket mengde sirkulerende leukocytter og sparsom utbredelse av Mott-lignede enkeltceller i vevet. Det ble ikke gjort funn av bakterier i dette materialet.
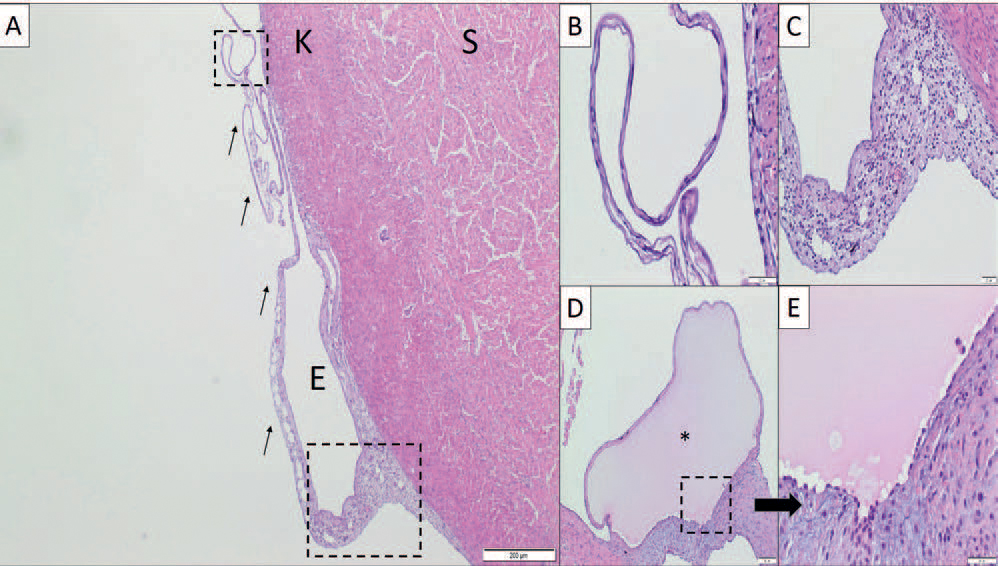
Figur 3. Histologisnitt av hjerte. A: Rester av cysteveggen (piler) kan sees på overflaten av epikardlaget (E) til ventrikkel. Kompaktlag (K), spongiøst lag (S). B: Høyere forstørrelse av rester av cystevegg i A, indikert med øvre firkant. C: Høyere forstørrelse av festepunkt på epikard i A, indikert med nedre firkant. D: Cyste (*) på en av AV-klaffene. E: Høyere forstørrelse av område markert med firkant i D. Målestokk 200 mm (A), 50 mm (D) og 20 mm (B, C og E). Bilde: Toni Erkinharju, Veterinærinstituttet.
Cyster er væskefylte kapsler av bindevev, og hos fisk dannes de ofte som respons på parasittinfeksjoner (1). Hos laksefisk er det imidlertid beskrevet flere cystetilstander uten klar parasittær etiologi, for eksempel polycystisk lever hos atlantisk laks (1) og polycystisk milt hos villfanget brunørret (Salmo trutta) i Skottland (1, 2). Etiologisk årsak for hjertecystene i vårt beskrevne tilfelle er ikke fullstendig klarlagt, men funn av lignende bakterier i cysteutstryk som i dype hudsår kan potensielt (om mulig) indikere en sammenheng med bakteriell septikemi.
Referanser
Roberts RJ. Fish pathology. 4th ed. Chichester: Wiley-Blackwell, 2012.
Roberts RJ, MacRitchie G. Multiple congenital splenic cysts in wild trout. J Wildl Dis 1971; 7: 155-6.
Systemisk toxoplasmose hos katt
Veterinærinstituttet
Ringerike Dyreklinikk
Veterinærinstituttet Oslo, seksjon for høyrisikoagens og patologi, mottok i juni 2020 en seks år gammel Sibirkatt (hann) fra Buskerud i Viken. Katten kom til veterinær i april 2019 på grunn av vekttap, og det ble påvist forhøyede nyreverdier i blodprøver. I februar 2020 hadde både vekt og nyreverdier normalisert seg. I begynnelsen av mai 2020 kom katten til veterinær for vaksinering. Den hadde gått noe ned i vekt, og eier hadde sett blod i pelsen rundt anus. Katten kom igjen til veterinær i slutten av mai fordi den hadde gått ytterligere ned i vekt og var dehydrert. Det ble ved ultralydundersøkelse påvist en forstørret krøslymfeknute, og ved eksplorativ laparatomi ble det tatt ut en liten biopsi som ble sendt til IDEXX for histologisk undersøkelse. Diagnosen på biopsien ble «sterk mistanke om lymfom med multifokal nekrose og infiltrasjon av nøytrofile granulocytter». En uke etter operasjonen ble katten dårlig og fikk væskebehandling hos veterinær. Den døde hjemme senere samme dag og ble sendt til obduksjon.
Ved obduksjonen var katten i normalt hold, blek og ikterisk. Det var stuvning og ødem i lungene, og leveren var orangerød. Milten var svullen og lys rød. I det ene nyret fantes multifokale nedsenkede faste områder i nyrebarken, og begge nyrer hadde fastere tekstur enn normalt. Magesekken var tom, og i tynntarmen fantes blodig slimet til tyntflytende innhold. I blindtarm og tykktarm var det rikelig med tørt fast lyst brunt innhold. Krøslymfeknutene var moderat forstørrede.
Histologisk undersøkelse av lever viste multifokale nekroser og rikelig forekomst av protozocyster forenlig med Toxoplasmagondii i hepatocytter og Kupfferceller (Figur 1). Spredte tachyzoitter fantes også i hjerne, myokard, lunge, lever, nyre, milt, tarm, krøslymfeknute og beinmarg. I hjernen var det infiltrasjon av mononukleære celler i meningene og multifokale små foci med betennelse i hjernevevet. I nyrene fantes multifokale områder med interstitiell fibrose og infiltrasjon av lymfocytter og plasmaceller. Bowmans kapsel og basalmembraner i tubuli var fortykkede, og det var degenerasjon og nekrose av både glomeruli og tubuli. I krøslymfeknute var det koagulasjonsnekrose. Det fantes lymfocytter i det perinodulære fettvevet, men cellene ble ikke vurdert til å være neoplastiske.
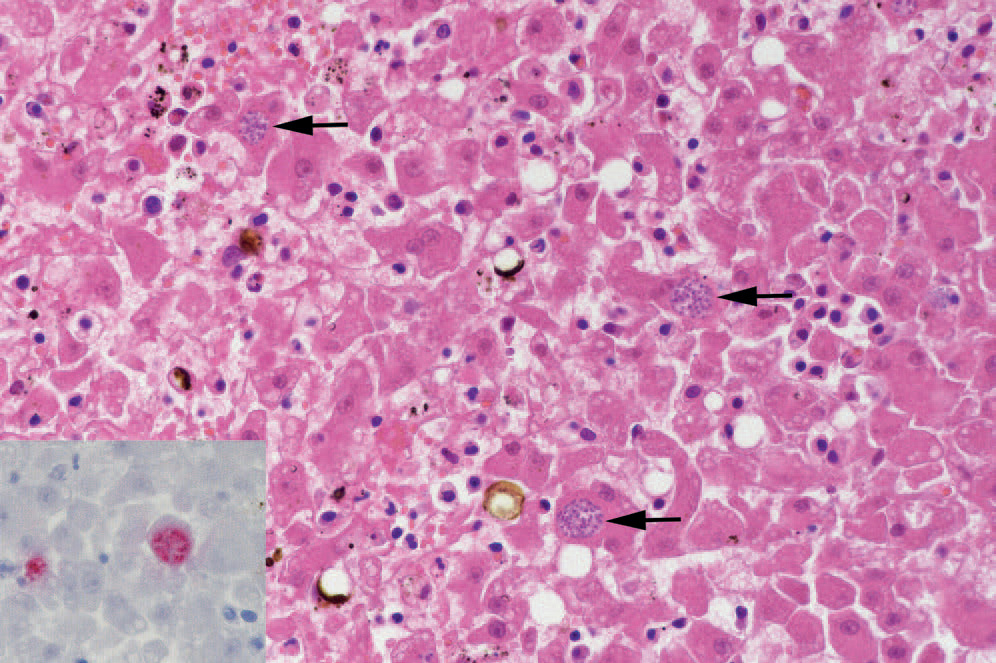
Figur 1. Histologisk snitt fra lever fra katt med multiple toxoplasmacyster i hepatocyttene (piler). Innfelt bilde viser positiv immunhistokjemisk farging (rød) for T. gondii. Foto: Helene Wisløff
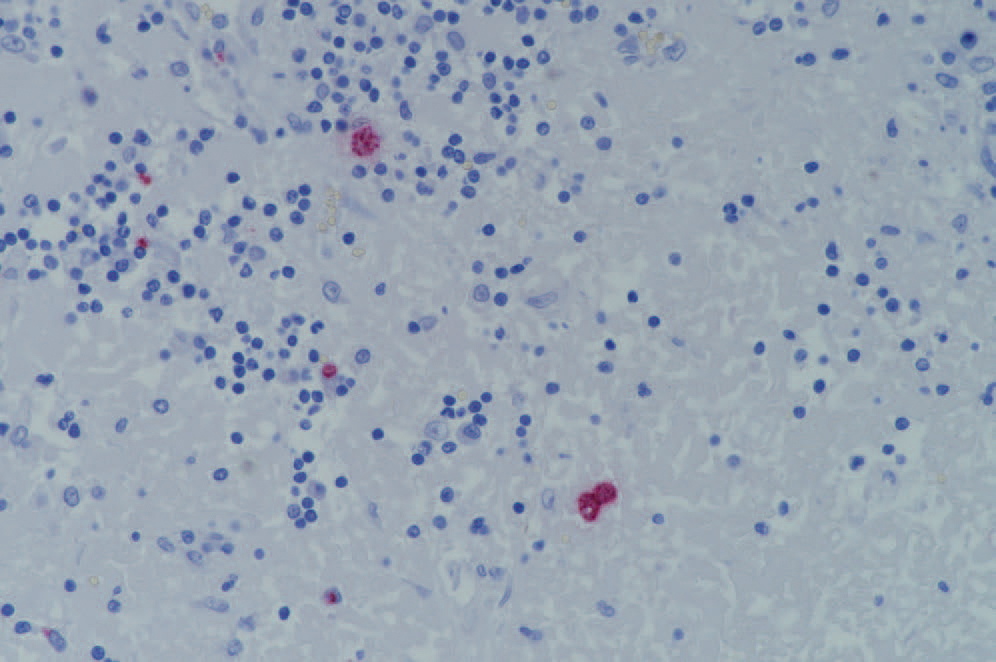
Figur 2. Histologisk snitt fra krøslymfeknute fra katt med multiple toxoplasmacyster. Bildet viser positiv immunhistokjemisk farging (rød) for T. gondii.Foto: Helene Wisløff
Immunhistokjemisk undersøkelse av hjerne, myokard, lunge, lever, nyre, milt, tarm, krøslymfeknute og beinmarg med hensyn på T. gondii ga positivt resultat, visualisert ved rød farge (Figur 2).
Katt er endevert for T. gondii, men kan også være mellomvert. Katter infiseres hovedsakelig ved å spise infiserte mellomverter som mus og fugl, men kan også smittes med oocyster i kattefaeces. Hos immunkompetente katter vil smitte føre til kjønnet og ukjønnet formering i tarmepitel og utskilling av oocyster i faeces. Som hos mellomvertene vil det også hos katt foregå en ekstraintestinal spredning av parasitten, men rask immunitetsutvikling vil føre til at cystene blir liggende i ulike vev uten å forårsake symptomer/sjukdom hos katten. Systemisk toxoplasmose kan forekomme hos nyfødte katter, unge immunologisk umodne katter og immunsupprimerte katter. Aktivering av dormante vevscyster kan for eksempel forekomme hos voksne katter som har fått immunosuppressiv behandling, eller katter som er infiserte med felint leukemivirus (FLV) eller felint immunsviktvirus (FIV).
I dette tilfellet ga biopsiundersøkelsen mistanke om at katten hadde lymfom. Dette kunne ikke bekreftes ved obduksjon og histologisk undersøkelse av indre organer. Forandringene i lymfeknutebiopsien var sannsynlig reaktive forandringer.
Muskeldegenerasjon hos kalv
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet, seksjon for høyrisikoagens og patologi, har i perioden 2018 - juni 2020 stilt diagnosen muskeldegenerasjon/nekrose på ti obduserte kalver og på innsendte organer fra to individ. Åtte av kalvene var kjøttfe, én var NRF, én var NRF/Telemarksblanding, mens rase ikke var oppgitt for de siste to kalvene. Av kjøttferasene var Charolais (3 stk.), Aberdeen angus (1), Hereford/Aberdeen angus (1), Dexter (1), Blonded’Aquitaine (1) og Highland cattle (1) representert.
Alderen på kalvene varierte fra nyfødt (død tre timer etter fødsel) til 2,5 måned. De fleste innsendelsene kom fra ulike fylker på Østlandet, mens en organinnsendelse var fra Trøndelag.
Bakgrunnen for innsendelsene var dødsfall hos flere kalver, opptil fem døde i noen besetninger. De fleste eiere hadde ikke registrert sykdomstegn, mens andre hadde registrert at kalvene ble slappe noen timer før de døde. I en anamnese var det oppgitt at flere kalver hadde dårlig sugerefleks, fikk navleinfeksjon og feber rett etter fødsel, og at den innsendte kalven ble avlivet da den lå på rygg med hodet bakover. Antibiotikabehandling hadde ingen effekt. En annen besetning hadde registrert diaré før kalvene døde. I de fleste rekvisisjonene ble fôringsregime ikke opplyst. I ett tilfelle ble det oppgitt at mordyrene ble fôret med dårlig grovfôr med mye halm og hadde fått Se/vitamin E bolus. I et annet tilfelle hadde dyrene kun fått grovfôr.
Ved obduksjon var alle kalvene dehydrerte og hadde lys lårmuskulatur, dels med kokt utseende (Figur 1). Hos flere kalver så en intermuskulært ødem. I hjertet fra fem kalver fantes lyse striper i myokard, og i tre andre hjerter var det blødninger. To av kalvene hadde i tillegg struma, én hadde nekrose i svelgslimhinnen, én hadde navleabscess og én hadde løpesår. Flere kalver hadde hyperemi i løpeslimhinnen og tynt innhold i tarmkanalen.
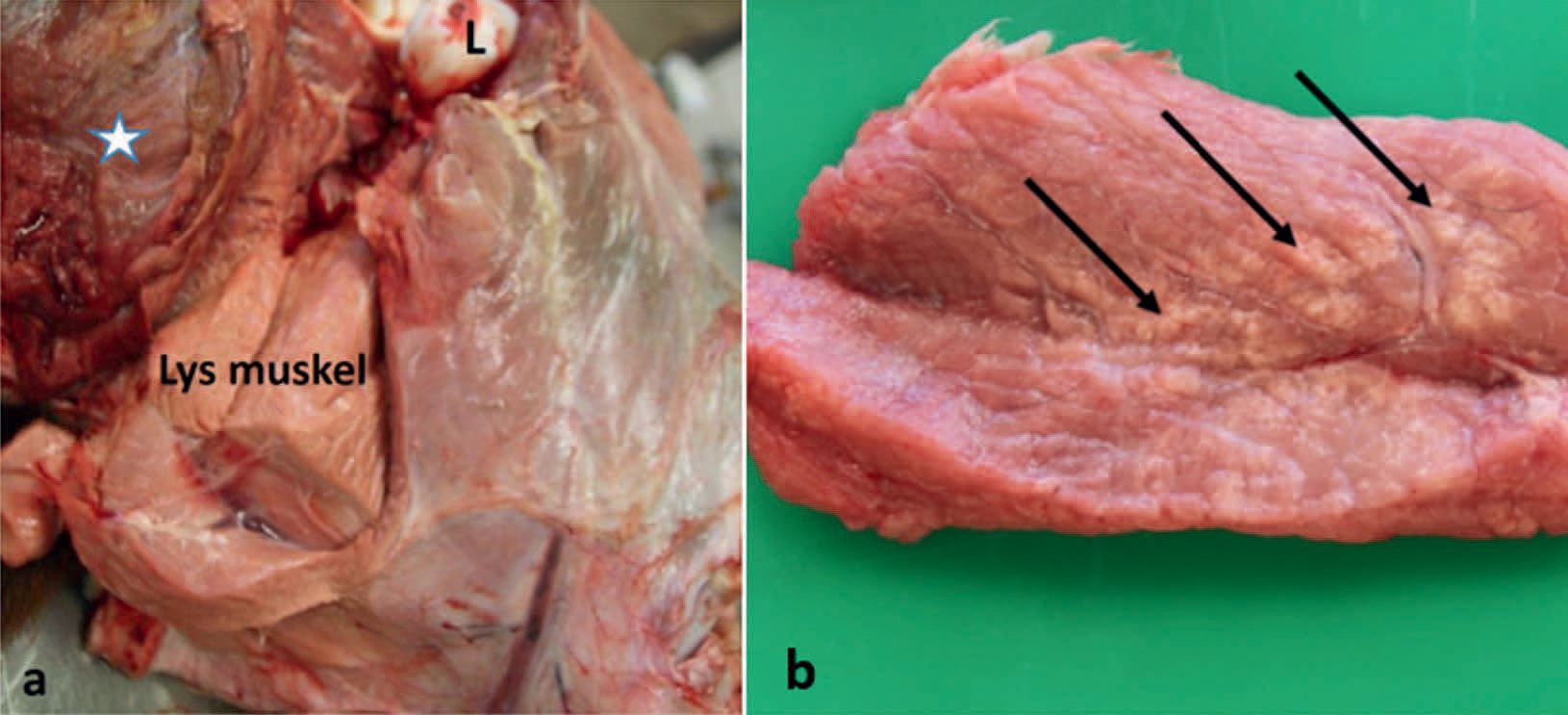
Figur 1 a og b. Lårmuskulatur fra kalv. 1 a viser lys og mørk muskulatur (stjerne). Lårhode (L). 1 b viser lårmuskulatur med flere lyse drag (piler). Foto: Øyvor Kolbjørnsen
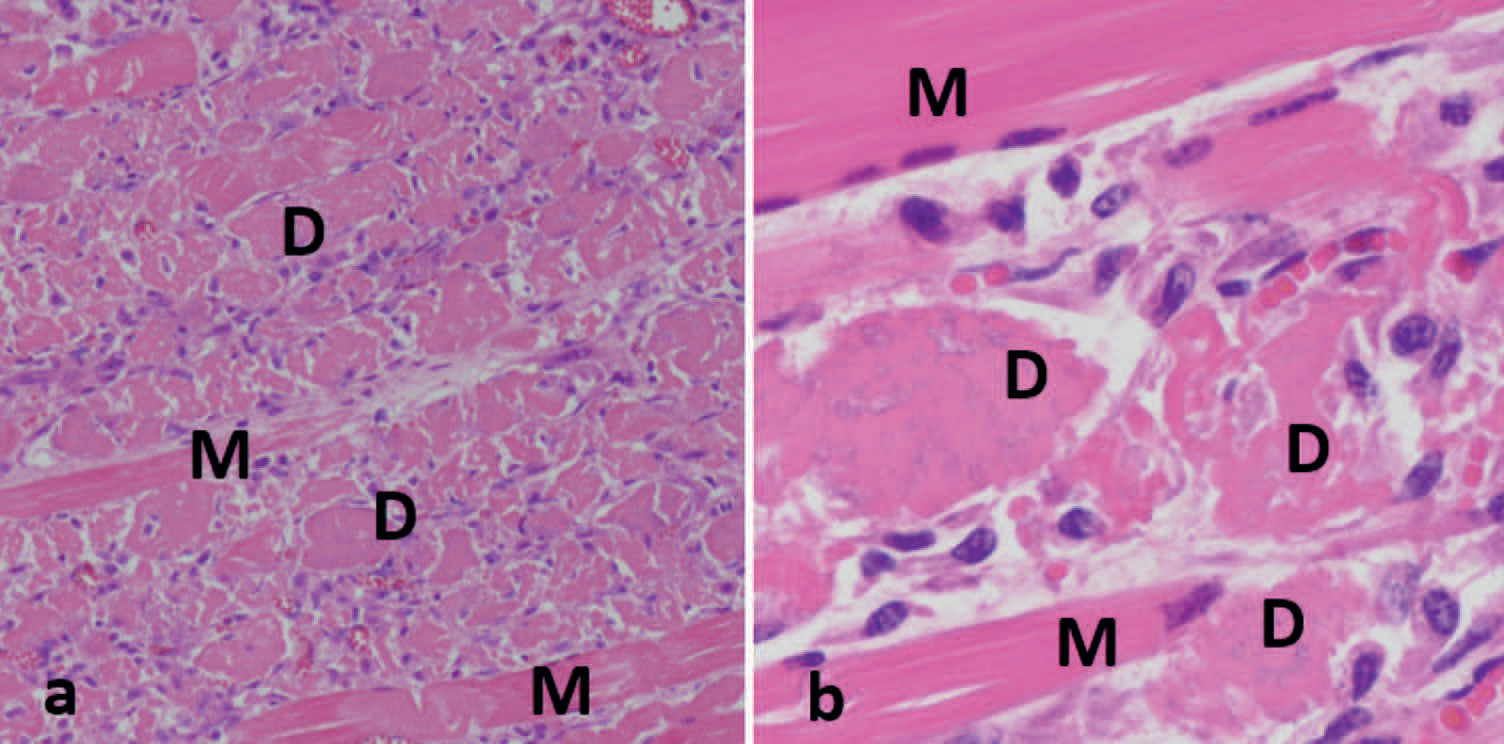
Figur 2 a og b. Histologisk preparat fra lårmuskulatur fra kalv. Figur 2 a viser et oversiktsbilde med uttalt muskeldegenerasjon og nekrose (D) og få normale skjelettmuskelfibre (M). Figur 2 b viser ved høyere forstørrelse et slikt område med svulne og nekrotiske fibre uten tverrstriping (D), svak mineralisering (multiple basofile granula) og en reaktiv cellerespons. Det er få normale muskelfibre med tverrstriping (M). Foto: Øyvor Kolbjørnsen
Ved histologisk undersøkelse fantes varierende grad av multifokal muskeldegenerasjon og nekrose med mineralisering (Figur 2). Myokard- og skjelettmuskelfibrene var hypereosinofile og svulne med tap av tverrstriping, fragmentert sarkoplasma og infiltrasjon av makrofager. I skjelettmuskulaturen ble det hos flere individ observert myofiberregenerasjon.
Ved bakteriologisk undersøkelse av tarminnhold fra mange av kalvene var det vekst av Clostridium perfringens eller Escherichia coli.
Ernæringsbetinget muskeldegenerasjon (EMD) hos kalv skyldes en kombinasjon av mangel på selen og vitamin E hos mordyret, noe som fører til at kalven ikke har tilstrekkelig nivå ved og etter fødsel. Selen (Se) er et mineral som inngår i en rekke enzymer, som sammen med vitamin E, beskytter cellemembraner, særlig i muskelceller. Selen er også viktig i kroppens omsetning av jod. Mangel kan gi svekket immunforsvar. Sykdomstegn hos kalv opptrer derfor oftest ved mangel på både selen og vitamin E, mens mordyret synes å ikke være affisert.
Norge har generelt lave nivåer av selen i jordsmonn og planter, både i innmark og utmark, og mangelen er størst i innlandet i Sør-Norge. Grovfôr på Vestlandet og langs kysten nordover inneholder noe mer Se, men ikke tilstrekkelig.
Storfe som har liten tilgang på kraftfôr, kan derfor ha lav selenstatus dersom ikke selentilskudd gis i tilstrekkelig mengde. Grovfôr av redusert kvalitet kan også gi mangel på vitamin E. Vitamin E finnes rikelig i ferskt gras og i grassurfôr som er riktig konservert. Behovet for tilskudd av vitamin E er større om vinteren og våren når dyrene får konservert fôr enn om sommeren og høsten.
Det er viktig å forebygge Se/vitamin E-mangel ved å fôre riktig og gi tilskudd til mordyr og til kalvene når de er gamle nok til annen ernæring enn melk.
Ved mistanke om EMD kan en ta blodprøver av mordyr for å undersøke selennivå (gjøres ikke på Veterinær-instituttet) eller sende inn døde kalver, eventuelt myokard og skjelett-muskulatur til Veterinærinstituttet for undersøkelse.
EMD er mest vanlig hos kalver alderen i 4-10 uker. Når skjelettmuskulaturen er mest angrepet, er kalvene ofte muskelsvake og stive og har problemer med å reise seg og stå. Hvis hjertemuskulaturen er angrepet, kan de vise anstrengt respirasjon. Plutselig død kan også inntreffe. Ungdyr med rask vekst, som hos kjøttfe, er særlig utsatt, men alle raser kan affiseres. EMD kan også sees hos aborterte og svakfødte kalver. EMD er angitt å opptre i forbindelse med utslipp på beite om våren, men flere av kalvene vi mottok, døde også i vintermånedene. Nivået av selen/vitamin E hos kalvene ble ikke undersøkt, men de patologiske forandringene var karakteristiske.
Ved tidlig behandling i besetninger med ernæringsbetinget muskeldegenerasjon hos kalv kan en gi Selevitan® vet. granulat eller injektabile, som inneholder både selen og vitamin E. Preparatene er forhåndsgodkjent og står på Statens legemiddelverks utleveringsliste.
Takk til alle praktiserende veterinærer som har sendt inn kalver og organer til obduksjon/undersøkelse. Dette bidrar til å sikre god kalvehelse og er et viktig bidrag til oversikten over vanlige sykdommer hos storfe.
Kråsbetennelse hos høns og kalkun
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Veterinærinstituttet
Nortura
Nortura
Nortura
Nortura
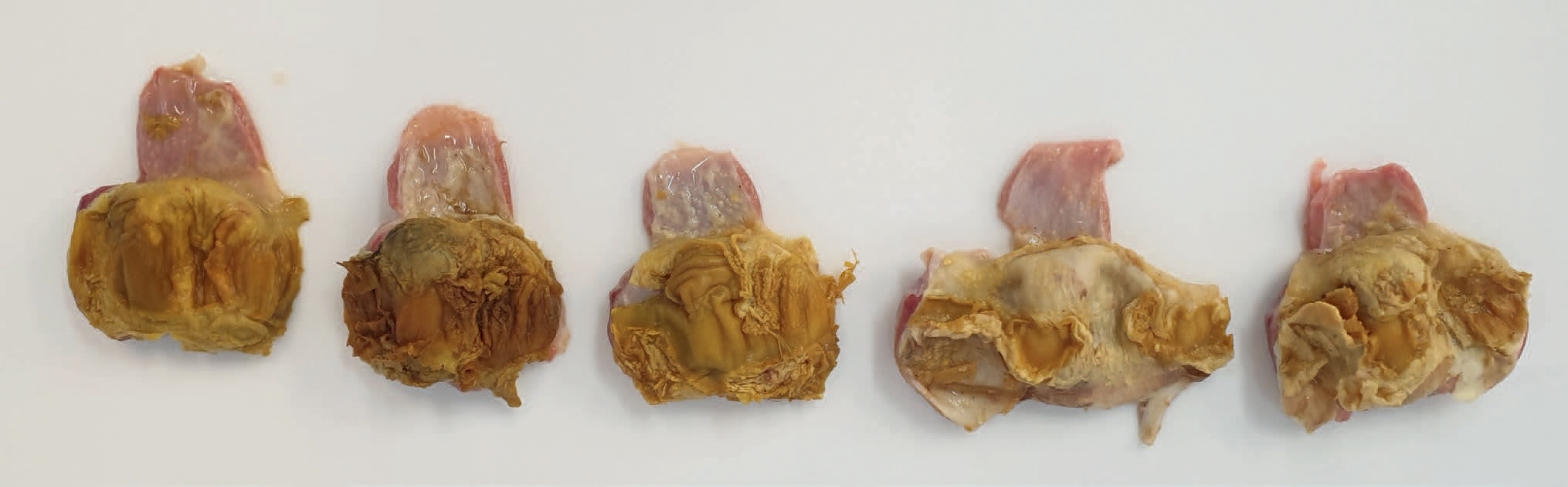
Figur 1 A: Krås og kjertelmage fra fem kalkunkyllinger, cirka tre uker gamle. Koilinlaget er fortykket, oppfliset, noe gallefarget og har delvis gått i oppløsning. På undersiden av koilinlaget er det lyst belegg. Foto: Helene Wisløff
Veterinærinstituttet, seksjon for høyrisikoagens og patologi, har i løpet av første halvår 2020 mottatt over 20 innsendelser med kyllinger av både høns og kalkun der hovedfunnet ved obduksjon har vært kråsbetennelse. Omtrent halvparten av innsendelsene har vært kadaver eller organer fra slaktekylling av rasen Ross 308. Alderen på kyllingene varierte fra tre dager til tre uker. Kråsbetennelse ble også påvist hos slaktekyllinger av rasen Ranger classic (alder 3,5 uke) og hos høns av rasene Lohmann hvit (alder 35 uker) og Dekalb (alder 39 uker). Knapt halvparten av innsendelsene var fra kalkun av rasen British United Turkey (BUT). Alderen på kalkunene varierte fra tre dager til cirka fem uker.
Det kliniske bildet i flokker som har problemer med kråsbetennelse, er ofte karakterisert av at dyra sturer, er rufsete i fjørdrakten, lite interessert i å bevege seg, stagnasjon i fôropptak og tilvekst og av og til forøket dødelighet.
Typiske makroskopiske forandringer som ble påvist i kråsen, var misfarget, fortykket, ujevnt og oppfliset koilinlag med lyse oppbløtte områder og sprekkdannelser/erosjoner (Figur 1). Koilinlaget løsnet ofte lett fra slimhinna, hvor det i en del tilfeller ble påvist erosjoner. Mengden innhold i kråsen varierte, og ofte var innholdet tørt og bestod hovedsakelig av flis. Av og til var innholdet gallefarget eller blodtilblandet.
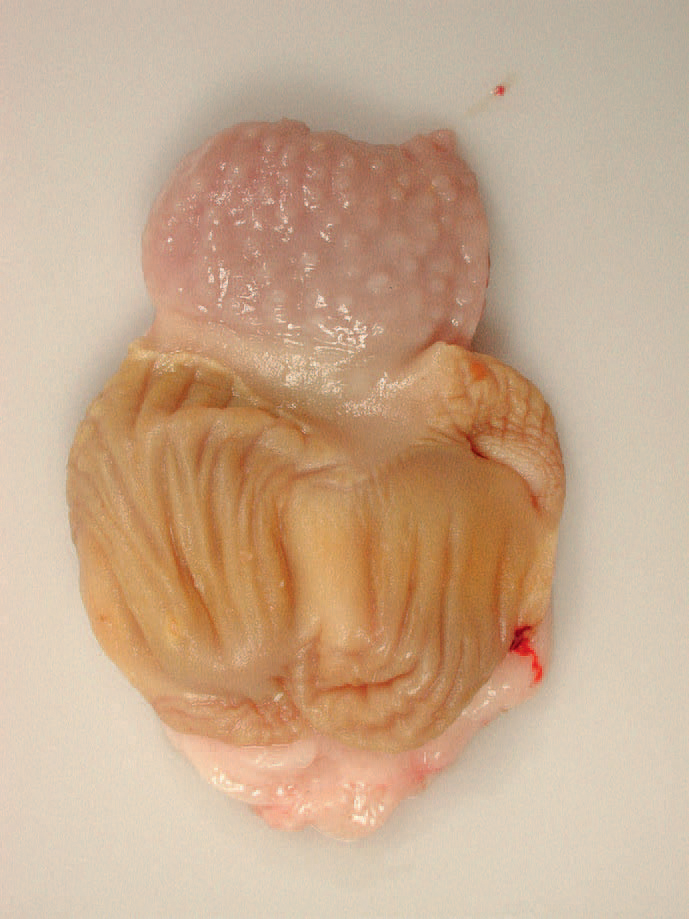
Figur 1 B: Normal krås og kjertelmage fra frisk slaktekylling. Foto: Veterinærinstituttet
Ved histologisk undersøkelse så man fortykket, eosinofilt og ofte spongiøst koilinlag med celledebris, leukocytter og rikelig med overveiende Gram-positive stavbakterier (Figur 2 A og B). I slimhinna fantes av og til dilaterte kjertler og i varierende grad infiltrasjon av leukocytter.
Ved bakteriologisk undersøkelse av kråsslimhinne/koilinlaget og tynntarm/blindtarm framkom i de fleste tilfellene rikelig vekst av Clostridium perfringens.
Årsaken til kråsbetennelse er ikke kjent, og det er usikkert om Cl. perfringens er den direkte årsaken eller om bakterien trives og vokser godt i et skadet koilinlag. Sannsynligvis er årsaken multifaktoriell. I litteraturen (Diseases of Poultry, 14th edition) er kråsbetennelse assosiert med adenovirusinfeksjon, men adenovirus har hittil ikke blitt påvist som årsak til kråsbetennelse hos høns og kalkun i norske besetninger. Antall innsendelser av slaktekylling og kalkun med alvorlig kråsbetennelse har økt i senere tid. Dette kan ha sammenheng med at bruken av koksidiostatika (narasin) til slaktekylling opphørte i 2016. Slaktekyllingene vaksineres nå mot koksidiose, men en ser likevel tilfeller med koksidiose i en del besetninger, noe som kan disponere for oppvekst av Cl. perfringens i tarmen.
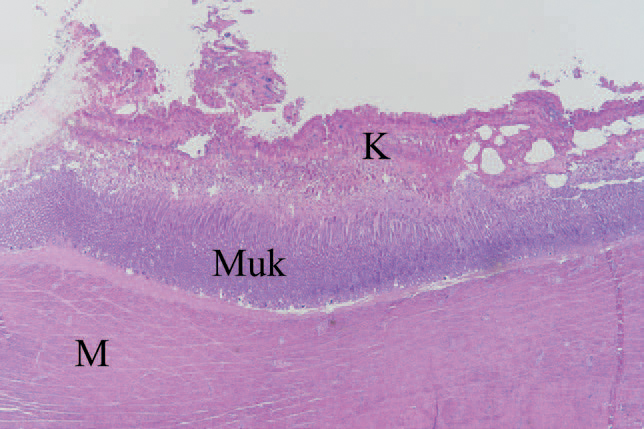
Figur 2 A: Histologisk snitt fra krås fra tre uker gammel kalkunkylling. Bildet viser uregelmessig spongiøst koilinlag (K) med rikelig med celledebris og leukocytter. M = muskellaget, Muk = mukosa. Foto: Helene Wisløff.
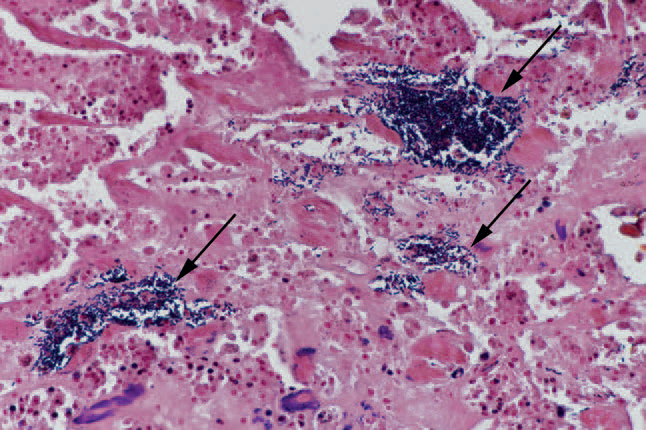
Figur 2 B: Gramfarget snitt fra samme krås som vist i 2A. Bildet viser nærbilde av koilinlaget med rikelig forekomst av Gram-positive stavbakterier (piler). Foto: Helene Wisløff
Tidligere forskning har vist at kråsbetennelse forekommer både i slaktekyllingflokker med og uten koksidiostatika i fôret (Kaldhusdal og Gjevre).
I konvensjonell kalkunproduksjon tilsettes fortsatt koksidiostatika (monensin) i fôret de første 8-9 ukene for å forebygge alvorlig tarmsjukdom fra koksidier, sikre god dyrevelferd og forhindre bruk av antibiotika (kilde: Animalia 2017), men det foregår nå et prosjekt med utfasing av monensin i kalkunproduksjonen. De fleste kalkuninnsendelsene til Veterinærinstituttet i 2020 har vært fra flokker som ikke har fått monensin i fôret. Det er likevel ikke sikkert at forekomsten av kråsbetennelse er høyere i flokker uten monensin enn i flokker med monensin i fôret, da terskelen for innsending av dyr fra monensinfrie flokker har vært lav.