Gjellesykdom: Uklare og forvirrende begreper
KUNNSKAP OM FISKEHELSE

I denne spalten vil Veterinærinstituttet i hvert nummer bidra med oppdatert kunnskap fra fiskehelsefeltet. Ansvarlig for spalten er fiskehelseansvarlig ved Seksjon for fiskehelse og biosikkerhet, Mona Gjessing - mona.gjessing@vetinst.no
Artikkelen nedenfor er tidligere trykket i Norsk fiskeoppdrett.
Gjellelidelser hos oppdrettslaks har i lang tid vært et alvorlig dyrevelferdsmessig problem. Det påvirker fiskens totale helse, og gir også store tap for næringen. Årsakene kan være mange. Gjelleproblemer kan skyldes sykdomsagens, miljøforhold, eller en kombinasjon av disse. Det mangler en entydig nomenklatur for karakterisering av gjellesykdom, noe som skaper forvirring og kan bidra til å forsinke oppklaring av slike sykdomstilfeller.
Sykdomsbegreper og diagnoser
Det benyttes i dag mange forskjellige betegnelser i forbindelse med gjellesykdom. Det kan for eksempel se ut som «proliferativ gjellebetennelse» (PGI) og «epiteliocystis» til dels brukes synonymt. Andre begreper som “haustsjuka”, “prikkesjuka”, «kronisk proliferativ gjellebetennelse», «proliferativ gjellesykdom» (PGD) og «multifaktoriell- » eller «kompleks gjellebetennelse» benyttes også noe om hverandre. Når vi skal lete etter tiltak for å unngå gjellelidelser eller i forbindelse med behandlinger, er det viktig å benytte mest mulig entydige begreper. Her vil vi vise noen eksempler som kan være uklare.
Epiteliocyster er en fellesbetegnelse på innkapslede bakteriekolonier inni epitelceller og her er det påvist ulike typer bakterier. De vanligste under norske oppdrettsforhold er antakelig Ca. Piscichlamydia salmonis og Ca. Branchiomonas cysticola. Særlig sistnevnte er assosiert med gjelleproblemer, men epiteliocyster kan også ligge inne cellene og se ut til å være harmløse.
«Epiteliocystis» en sykdomsbetegnelse som gjerne brukes ved tilstander der man antar at det er epiteliocystene som er årsak til gjellesykdom. I noen tilfeller er omfanget av epitelicyster så omfattende (vurdert ved histopatologi) at det er grunn til å tro at de skaper problemer og da er det antakelig riktig å bruke begrepet «epiteliocystis». Sykdomsbetegnelsen «epiteliocystis» brukes også noen ganger når epiteliocyster blir påvist (ved histopatologi) samtidig med gjelleskade (makroskopisk synlig eller histopatologisk), men uten at man kan være sikker på at bakteriene er årsak til gjelleforandringene. Smitteforsøk tyder på at det er en sammenheng mellom Ca. Branchiomonas cysticola og gjellesykdom med betennelsesceller og økt antall epitelceller. Dette er imidlertid en generell reaksjon som kan ha flere forklaringer. Derfor er det grunn til å være varsom med diagnosen «epiteliocystis» i slike tilfeller.
«Haustsjuka» («prikkesjuka») oppstod da man høsten 2008 så flere utbrudd der fisken hadde betennelse og vevsdød/nekrose («prikker») i gjellene. Samtidig var det forandringer inni fisken som blødninger, betennelse, nekrose og sirkulasjonsforstyrrelse. Mistanken om årsak til forandringene falt på mikrosporidien Desmozoon lepeophtherii.
«Proliferativ gjellebetennelse» («proliferative gill inflammation»/PGI) ble i sin tid beskrevet ut fra en spesifikk kombinasjon av histopatologiske funn alene uten å forholde seg til eventuelle agens som finnes der. Betegnelsen har til en viss grad blitt misoppfattet som synonymt med «epiteliocystis».
«Amøbegjellesykdom» eller AGD, forårsakes av amøben Paramoeba perurans, men sees ofte sammen med andre agens og skader på gjellene.
Komplekse årsaksforhold kan gjøre valg av terminologi vanskelig
Det er bare unntaksvis at vi er sikre på hvilke bakterier, virus, parasitter, alger, maneter, miljøfaktorer eller kombinasjoner av disse, som gir skadene vi ser. Det er med andre ord vanskelig å si noe sikkert om årsak og virkning.
Når det gjelder sykdomsdiagnoser, så er det få klart definerte når vi snakker om gjeller. To eksempler er AGD og «laksepox» som skyldes salmon gill pox virus (SGPV). Ved AGD er vevsendringene forholdsvis typiske og dersom det blir observert amøber med typisk morfologi for Paramoeba i tilslutning til slike lesjoner, settes en spesifikk sykdomsdiagnose. Også for «laksepox» er det svært typiske funn, men det er anbefalt å støtte de histopatologiske funnene med positiv PCR for SGPV.
Kompleks gjellesykdom eller gjellelidelse (CGD – complex gill disease eller complex gill disorder) er begreper som mer og mer er tatt i bruk og er definert som histopatologiske funn som gir grunn til å tro at det er mer enn en årsak til sykdomsforandringene (figur 1, 1a-d)1. Særlig hos fisk som prøvetas etter at den er blitt klinisk syk, vil gjelleforandringene være så omfattende at det er vanskelig å si hva som kom først og sist. De histopatologiske funnene er da ofte sammensatte og trolig resultat av en varierende kombinasjon av agens (bakterier, virus, parasitter), miljø og håndtering.
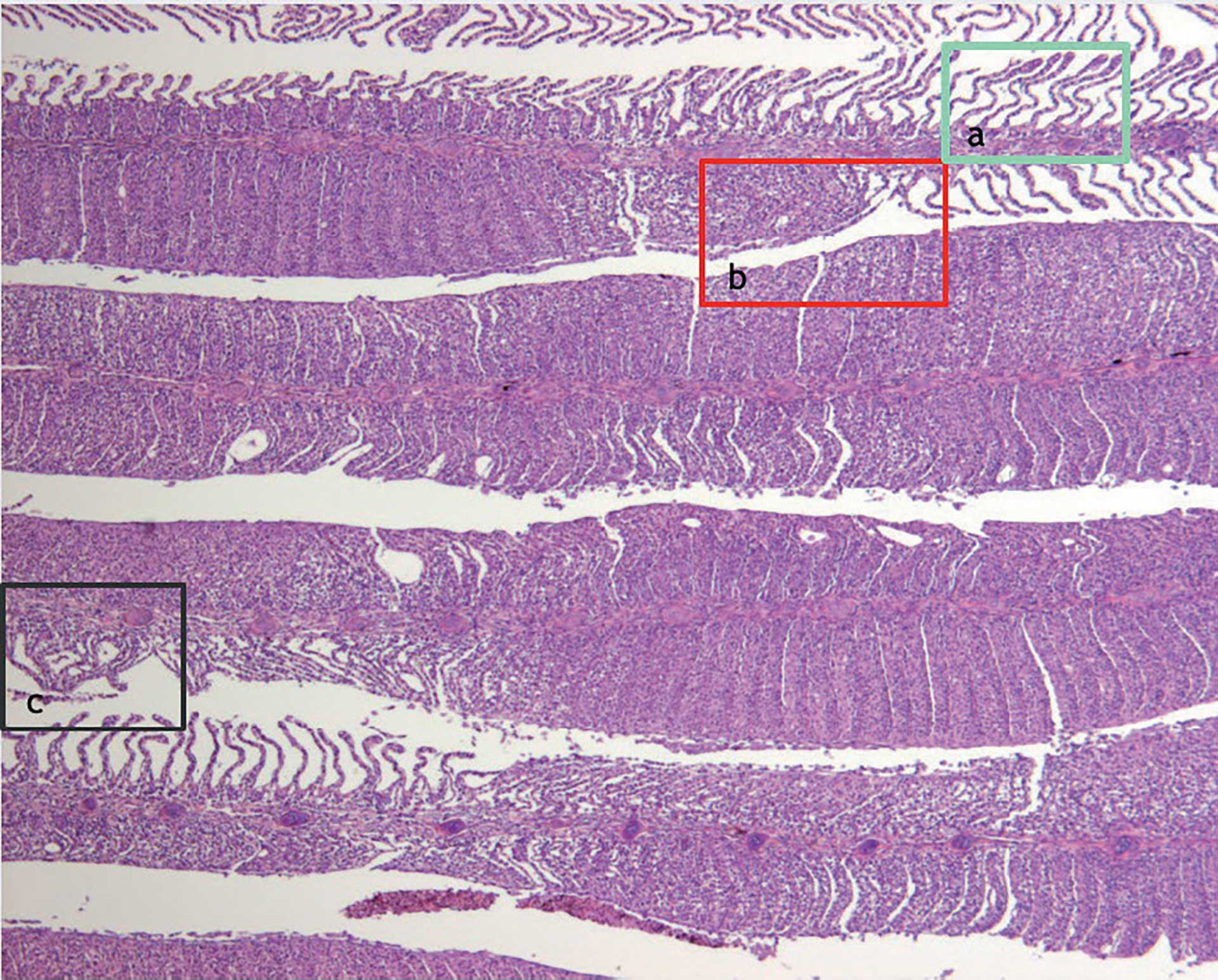
Figur 1. Oversikt over gjelle med ulike typer forandringer. Ved første øyekast minner forandringene om det vi ser ved AGD, men her er det, i tillegg til amøber, andre agens som skaper problemer. Behandling mot AGD vil kanskje i dette tilfelle gjøre mer skade enn det motsatte. Se områder i grønn, rød og svart boks som er forstørret i bilder under.
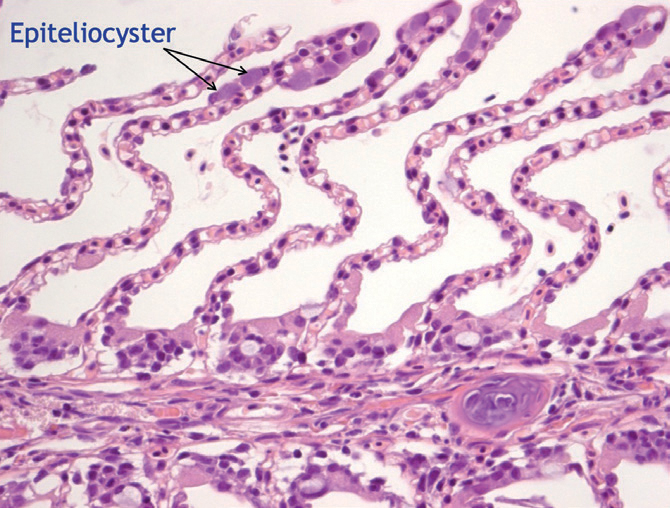
Figur 1a. Område fra figur 1 (område a) som er forstørret.
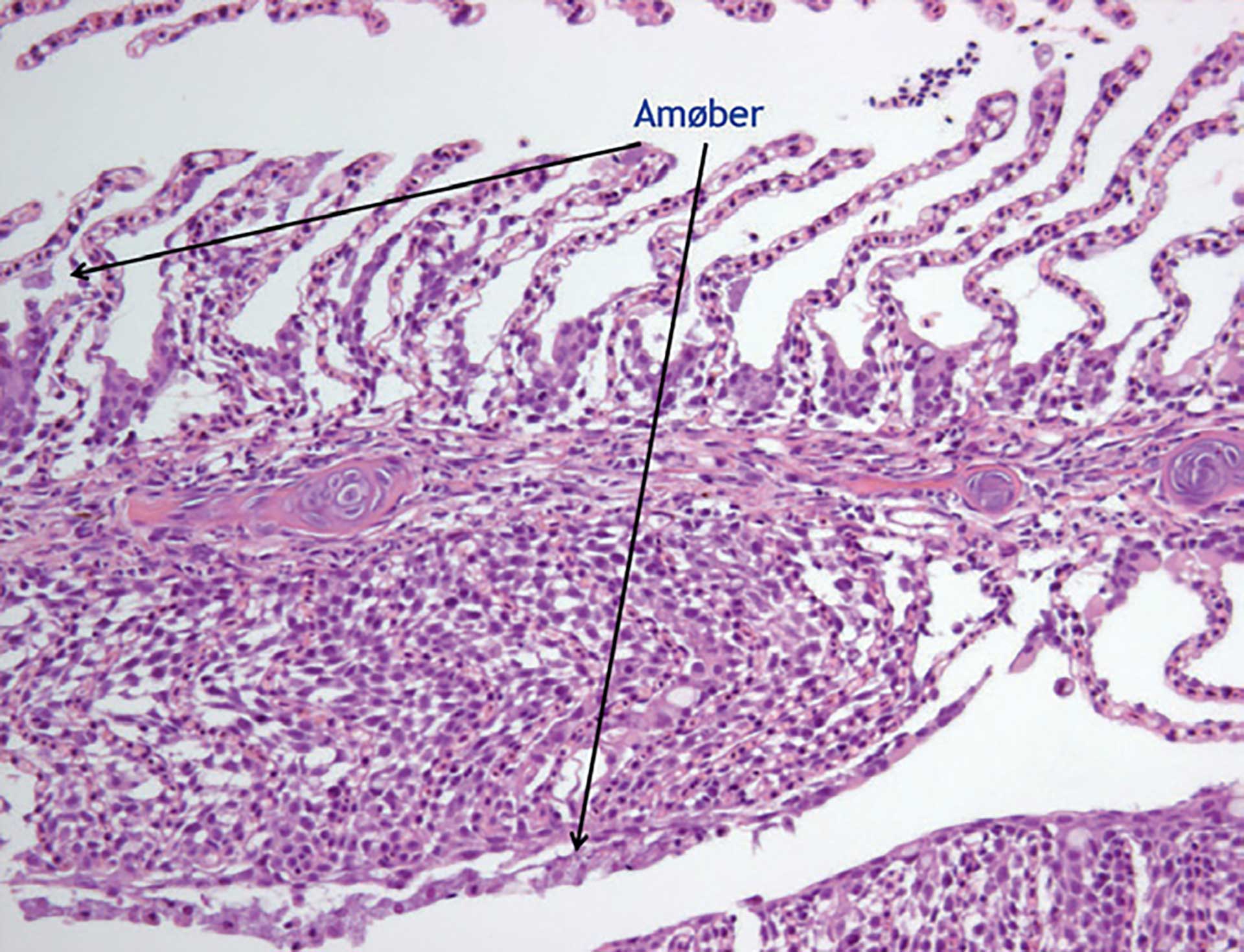
Figur 1b. Område fra figur 1 (område b) som er forstørret.
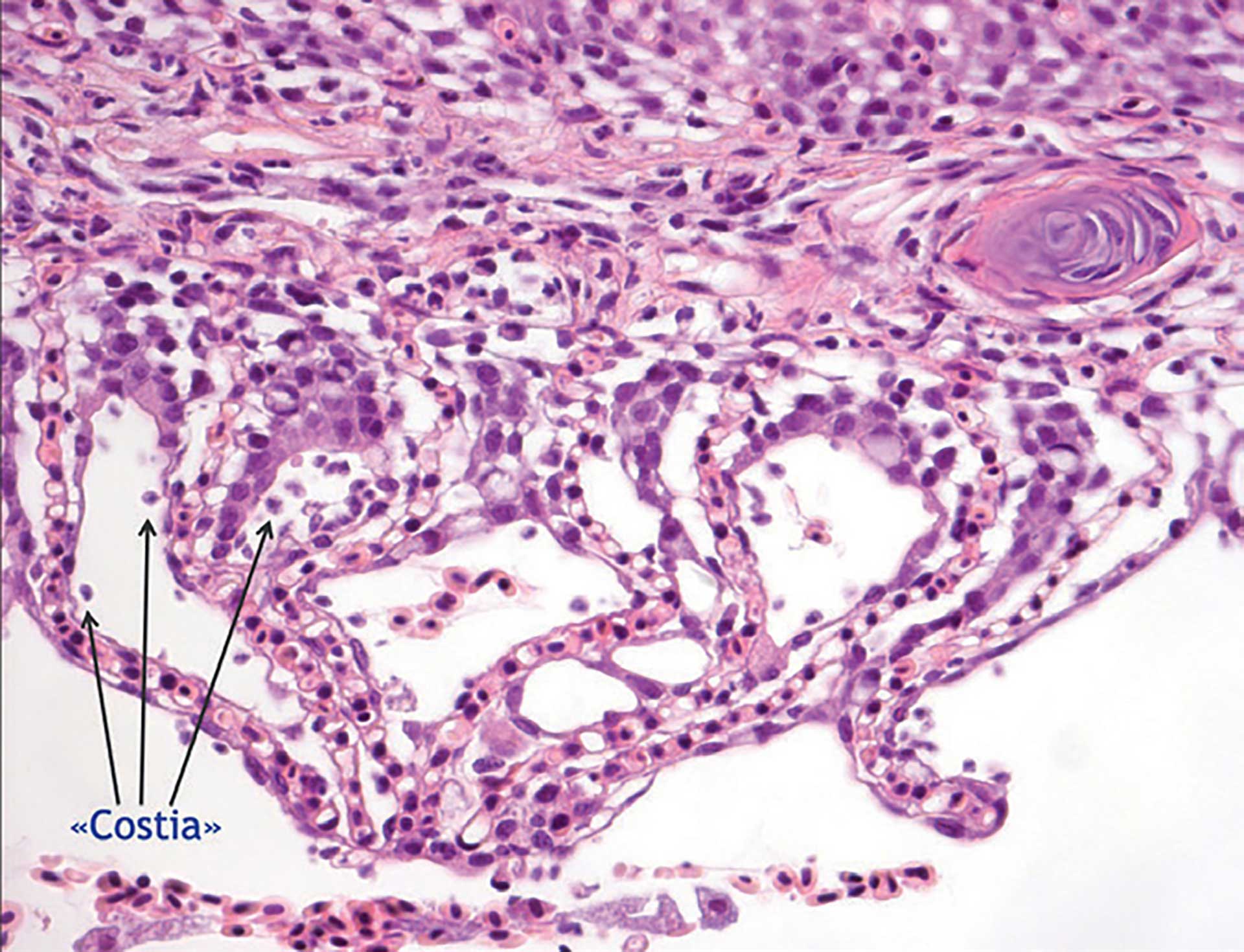
Figur 1c. Område fra figur 1 (område c) som er forstørret.
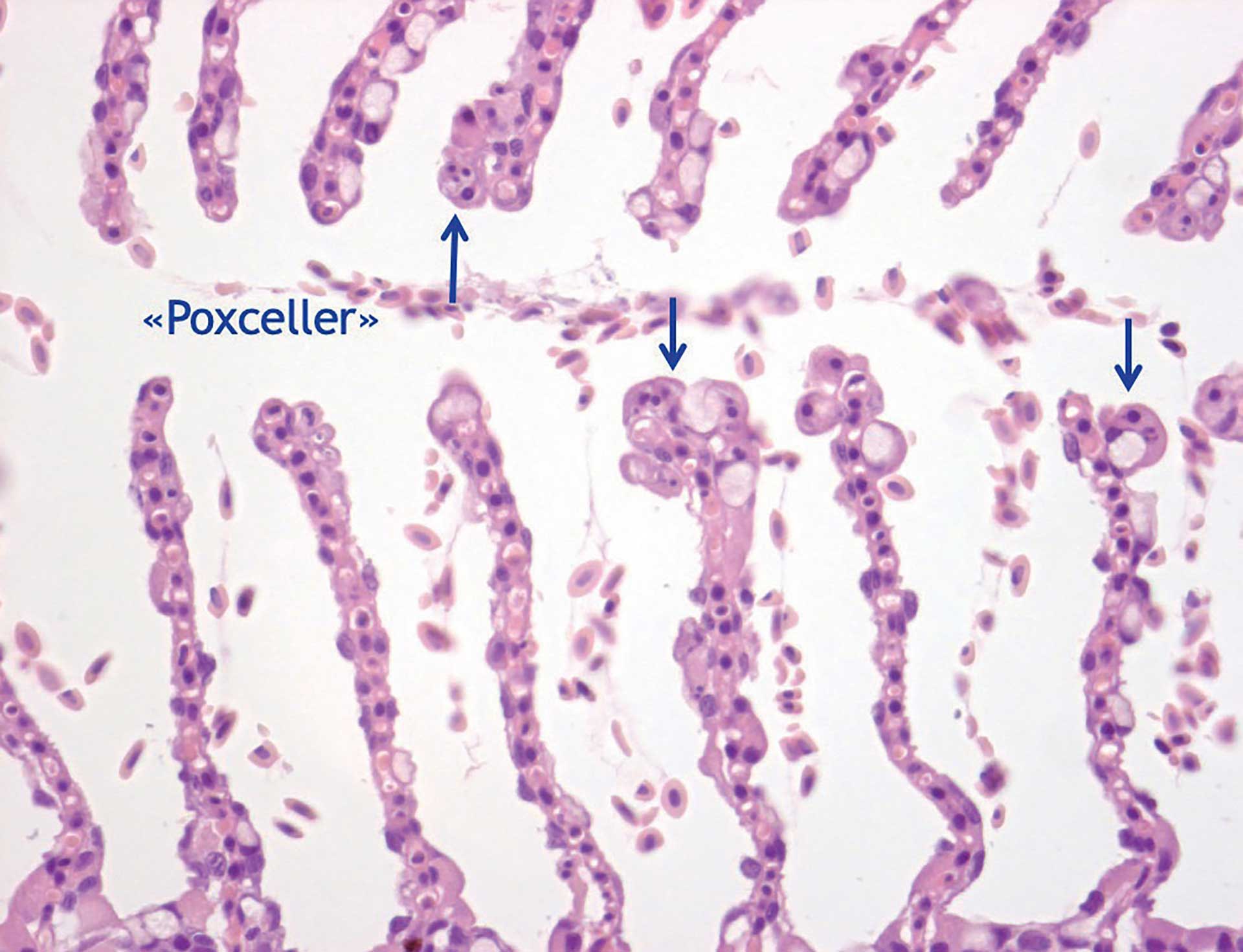
Figur 1d. Område fra samme gjelle som i figur 1 for å vise at her var det også tegn på at laksepoxvirus var tilstede. Dette ble også bekreftet ved pcr.
Det er viktig at hoveddiagnosen er entydig, og at begrepet «kompleks gjellesykdom» benyttes hvis forandringene er sammensatte og det trolig er flere årsaker. Laboratoriene bør da, i den grad det er mulig, peke på mulige årsaksforhold som kan være involvert.
Det er behov for mer kunnskap
Det er store kunnskapshull når det gjelder årsaker til gjelleproblemer og hva som utløser de forskjellige vevsreaksjonene. Selv om det finnes flere kjente agens/mikrober, mangler det vesentlige verktøy for å avdekke hvilke egenskaper disse har, hvordan de enkeltvis eller sammen påvirker fisken, smittsomhet og så videre. Mange av smittestoffene har man ennå ikke lyktes med å dyrke og det gjenstår å utvikle reproduserbare smittemodeller for eksperimentelle studier.
Et godt samarbeid mellom fiskehelsepersonell som arbeider i felten og diagnoselaboratoriene er viktig for å kunne komme videre i en felles beskrivelse av gjellesykdommer. I 2018 ga Veterinærinstituttet ut en rapport som blant annet omhandlet standardisering av AGD-gjellescore2. Det er FoMas fiskehelse og miljø som har utarbeidet standarden for «AGD-score» og «total gjellescore». Data fra eksperimentelle forsøk viser at metoden er både praktisk gjennomførbar og reproduserbar og gir et godt bilde av graden av synlige (makroskopiske) gjelleforandringer. En slik bedømmelse kan danne grunnlag for vurdering av gjelleskaden, eventuelt behov for behandling, spesielt med tanke på AGD, og vurdering av resultatene av en behandling.
Nå er det også publisert et scoringsystem for vurdering av histologiske gjelleforandringer3. Det gjenstår å optimalisere undersøkelsesmetodene for gjeller slik at resultatene gir et riktigst mulig bilde av situasjonen med hensyn på årsak(er), alvorlighetsgrad og mulighetene for å forebygge eller behandle. Det er viktig at prøver for histologisk undersøkelse tas ut på riktig måte. De ulike smittestoffene eller annet som påvirker gjellene, rammer kanskje ikke gjellene på samme sted. Det kan føre til at dersom prøvene som undersøkes ikke omfatter de mest aktuelle partiene, kan en gå glipp av viktige lesjoner.
Samtidig med at gjelleunder-søkelsene kan gi oss mer informasjon om det som skjer i gjellene, må vi også rette blikket mot miljøet for å få bedre oversikt over hva oppdrettsfisken faktisk utsettes for og sette disse observasjonene i sammenheng med øvrige funn.
Referanser:
Noguera P, Olsen AB, Hoare J, Lie KI, Marcos-López M, Poppe TT, Rodger H. Complex gill disorder (CGD): a histopathology workshop report. Bull Eur Assoc Fish Pathol 2019; 39: 172-6.
Hytterød S, Kristoffersen AB, Mari Darrud M, Kolstø S, Mo TA, Blindheim SH et al. Standardisering av AGD-gjellescore. Enhetlig gjellescoring basert på data fra eksperimentelle forsøk og oppdrettsanlegg for laks. Oslo 2018. (Veterinærinstituttet. Rapport 19 - 2018).
Gjessing MC, Steinum T, Olsen AB, Lie KI, Tarvornpanich S, Colquhoun DJ et al. Histopathological investigation of complex gill disease in sea farmed Atlantic salmon. PLoS One 2019; 14: e0222926.