Ny behandling av felin infeksiøs peritonitt (FIP)
Felin infeksiøs peritonitt (FIP) er forårsaket av infeksjon med kattens koronavirus (FCoV), et enkeltstrenget RNA-virus. Infeksjon med FCoV er utbredt hos katter. Enkelte utvikler en mild diaré, mens andre gjennomgår infeksjonen subklinisk. Hos noen få katter oppstår en mutasjon i FCoV som gir viruset affinitet for monocytter og makrofager, dermed kan de utvikle den alvorlige sykdommen vi kjenner som FIP.
FIP har inntil nylig blitt regnet som 100 % dødelig. I kjølvannet av covid-19-pandemien er det utviklet nye antivirale medisiner mot infeksjon med koronavirus. Nukleosidanalogene remdesivir og GS-441524 har vist seg å være effektive medisiner også mot FIP. I denne artikkelen presenteres anbefalinger for behandling og oppfølging av katter med FIP, to katter med FIP behandlet med GS-441524 og virkningsmekanismen for denne medisinen.
Spesialist i smådyrsykdommer – hund og katt, EMPET Stabekk AS
Veterinær, EMPET Stabekk AS
GPCert(SAS), spesialist i smådyrsykdommer – hund og katt
Daglig leder ved EMPET Stabekk AS
Innledning
Kattens koronavirus (FCoV) er et kappekledd enkelttrådet positiv sens ribonukleinsyre (RNA)-virus som tilhører familien Coronaviridae i ordenen Nidovirales. FCoV tilhører slekten alfakoronavirus sammen med blant annet hundens koronavirus (CCoV), mens severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) tilhører slekten betakoronavirus. Det karakteristiske utseende er opphavet til navnet «corona», som betyr krone eller krans på latin. Som følge av covid-19-pandemien er medisinen GS-441524 nå tilgjengelig for veterinærmedisinsk bruk. Endelig er det mulig å behandle sykdommen felin infeksiøs peritonitt (FIP) (1,2).
Patofysiologi
Infeksjon med FCoV er utbredt blant katter. De fleste gjennomgår infeksjonen subklinisk, men noen utvikler mild til alvorlig enteritt. Kattene er smittebærende i to til tre måneder. Immuniteten varer ikke lenge, og kattene kan reinfiseres bare noen uker senere. Omtrent 5 % av kattene med FCoV-infeksjon i en større kattepopulasjon utvikler FIP. Det er ikke helt klarlagt hvorfor noen katter utvikler sykdommen. Den rådende teorien er at viruset gjennomgår mutasjoner i katten, som resulterer i endring av affinitet fra enterocytter til monocytter og makrofager. Det er en kombinasjon av virulensen til FCoV, mengden virus, og kattens immunrespons som avgjør om den utvikler FIP. Vanligvis vil virale antigener på overflaten av cellen resultere i en antistoff- eller cellemediert lysis av den infiserte cellen. Hos katter med FIP vises ikke det virale antigenet på overflaten og de infiserte cellene unngår dermed celledød. Monocyttene går ut i vevet hvor de omdannes til makrofager. Ved akutt FIP er flere blodkar affisert, samtidig som en kraftig antistoffrespons fører til økt permeabilitet i kapillærene. Lekkasjen av plasma fører til effusjoner og det klassiske «våt FIP» forløpet. Ved de mer kroniske formene for FIP er færre blodkar involvert og det er i mye større grad en cellemediert respons som fører til perivaskulære pyogranulomer, også kalt «tørr FIP» (1,2).
Kliniske tegn på FIP
De aller fleste katter som blir diagnostisert med FIP er unge katter under to år, men katter i alle aldre kan få sykdommen. Det ser ut til at rasekatter har høyere risiko for å utvikle FIP. Om dette er en genetisk svakhet eller om det er stressrelatert er ikke kjent. Det er ikke uvanlig at kattene som utvikler FIP presenterer med en anamnese hvor de er blitt utsatt for stress, som for eksempel kastrering, drektighet eller opphold på kattepensjonat (1,2).
Kliniske tegn varierer avhengig av hvilket organ eller organer som er affisert, og om det i hovedsak er en vaskulopati som resulterer i effusjoner («våt FIP») eller en granulomatøs form med dannelse av (pyo)granulomer i ulike organer («tørr FIP»). Det behøver ikke være enten eller, granulomer kan finnes ved «våt FIP», og ved granulomatøs FIP kan ascites utvikles (1). I en retrospektiv studie med 231 katter med FIP hadde 78 % av kattene ascites (3).
Katter med FIP har gjerne uspesifikke kliniske tegn på nedsatt allmenntilstand som feber, letargi, anoreksi og vekttap. De fleste kattene med FIP har letargi (over 80 %), og over halvparten av kattene har feber og anoreksi (1,3). Ved den typiske «våte» formen for FIP vil det være abdominal distensjon grunnet ascites, men effusjoner andre steder som i pleura og perikard er også mulig. FIP kan gi sykdom i de fleste organsystemer, eksempelvis uveitt, renomegali, pyogranulomatøs pneumoni, lymfadenomegali, proteintapende enteropati, hudforandringer med kuler med eller uten kløe, myokarditt og nevrologiske forandringer (1). Katter med nevrologiske tegn (ataksi, anfall, vestibulært syndrom, parese, paralyse og somnolens) utgjorde 18 % av tilfellene i en studie med 231 katter (3). Andre studier har funnet nevrologiske tegn hos opptil 30 % av katter med FIP. FIP er også en kjent årsak til uveitt hos unge katter. I studier gjort på katter med uveitt i USA og Storbritannia var FIP den nest vanligste årsaken, og utgjorde 16 % av tilfellene. Den vanligste årsaken var idiopatisk uveitt (1). Uten behandling dør kattene vanligvis i løpet av noen uker etter å ha fått påvist FIP. Før remdesivir ble tilgjengelig hendte det imidlertid at enkelte katter overlevde måneder og av og til år med diverse behandlinger (NSAIDs, immunstimulerende medikamenter, interferon, og/eller kortison), men det kunne ikke bevises at denne behandlingen var årsak til forlenget overlevelse (1,2).
Diagnostikk
Det finnes ikke én enkelt diagnostisk test som sikkert kan påvise FIP. Diagnostisering av sykdommen handler om å sette anamnese, kliniske tegn og ulike prøvesvar i sammenheng. Typiske funn på generelle blodprøver er økt serumglobuliner, eventuelt lavt serum albumin, som resulterer i en lav albumin/globulin ratio (<0,6). Et annet typisk funn er hyperbilirubinemi. Ved hematologisk undersøkelse er det vanlig å finne en non-regenerativ anemi, lymfopeni, nøytrofili og trombocytopeni. Billeddiagnostikk vil kunne påvise fri væske i buken, perikard eller pleura ved «våt FIP», eller tegn til nodulære forandringer i organer eller krøs ved granulomatøs FIP (1,2).
Ved prøvetaking av fri væske i buk, pleura eller perikard fås typisk en væske med gul farge som virker trådtrekkende. Proteinnivået av denne væsken er ofte høy (>35 g/L), og har moderat til lavt celleantall. Cytologisk evaluering av denne væsken viser et inflammasjonsbilde med overvekt av makrofager og nøytrofile granulocytter. Rivalta test er en enkel test for å skille mellom transudat og eksudat. Testen utføres ved at et reagensglass fylles ¾ fullt med destillert vann og 1 dråpe 98 % eddiksyre. Deretter dryppes en dråpe effusjonsvæske i reagensrøret. Om dråpen går i oppløsning og væsken fortsetter å være transparent er testen negativ (transudat) og FIP er usannsynlig. Om dråpen holder formen sin og ligger igjen på overflaten eller sakte faller nedover mot bunn er testen positiv (eksudat) og FIP mer sannsynlig (1,2).
Dersom kliniske tegn (Figur 1) og analyser av effusjon (Figur 2) peker mot FIP, bør væske og/eller vevsprøver undersøkes for FCoV- RNA. FIP er svært sannsynlig dersom kvantitativ FCoV RT-PCR (revers transkriptase polymerase kjedereaksjon) er positiv med store mengder FCoV- RNA antigen i effusjonsvæsken, eller dersom immuncytokjemi for påvisning av FCoV-antigen er positiv. Histopatologi forenlig med FIP (pyogranulomatøse forandringer), kombinert med positiv FCoV-antigen på immunhistokjemi er angitt å være godt nok for å stille diagnosen FIP. Et negativt utslag på FCoV-antigen utelukker dessverre ikke FIP. Pasienten må da fortsatt monitoreres for å se om det utvikler seg abnormaliteter det kan tas nye prøver av med enten FNA, tru-cut eller kirurgisk fulltykkelses biopsi. Antistofftester har liten diagnostisk verdi fordi testene ikke skiller mellom antistoffer utviklet mot lavvirulente FCoV som gir mild enteritt og høyvirulente FCoV som gir FIP (1,2).
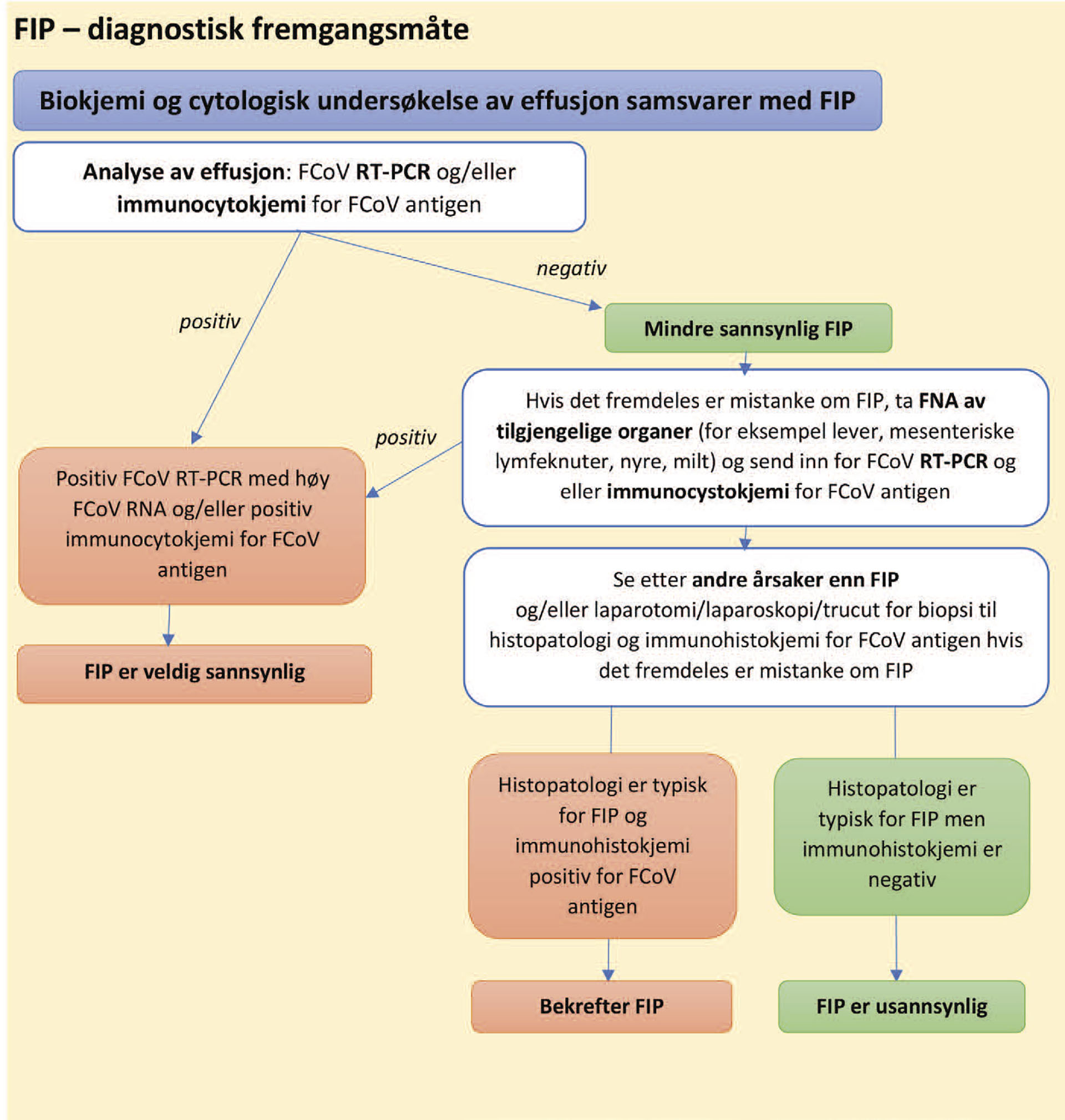
Figur 1: Diagnostisk fremgangsmåte for FIP ved effusjon. Figur er hentet fra Tasker et al 2023 og oversatt til Norsk (1).
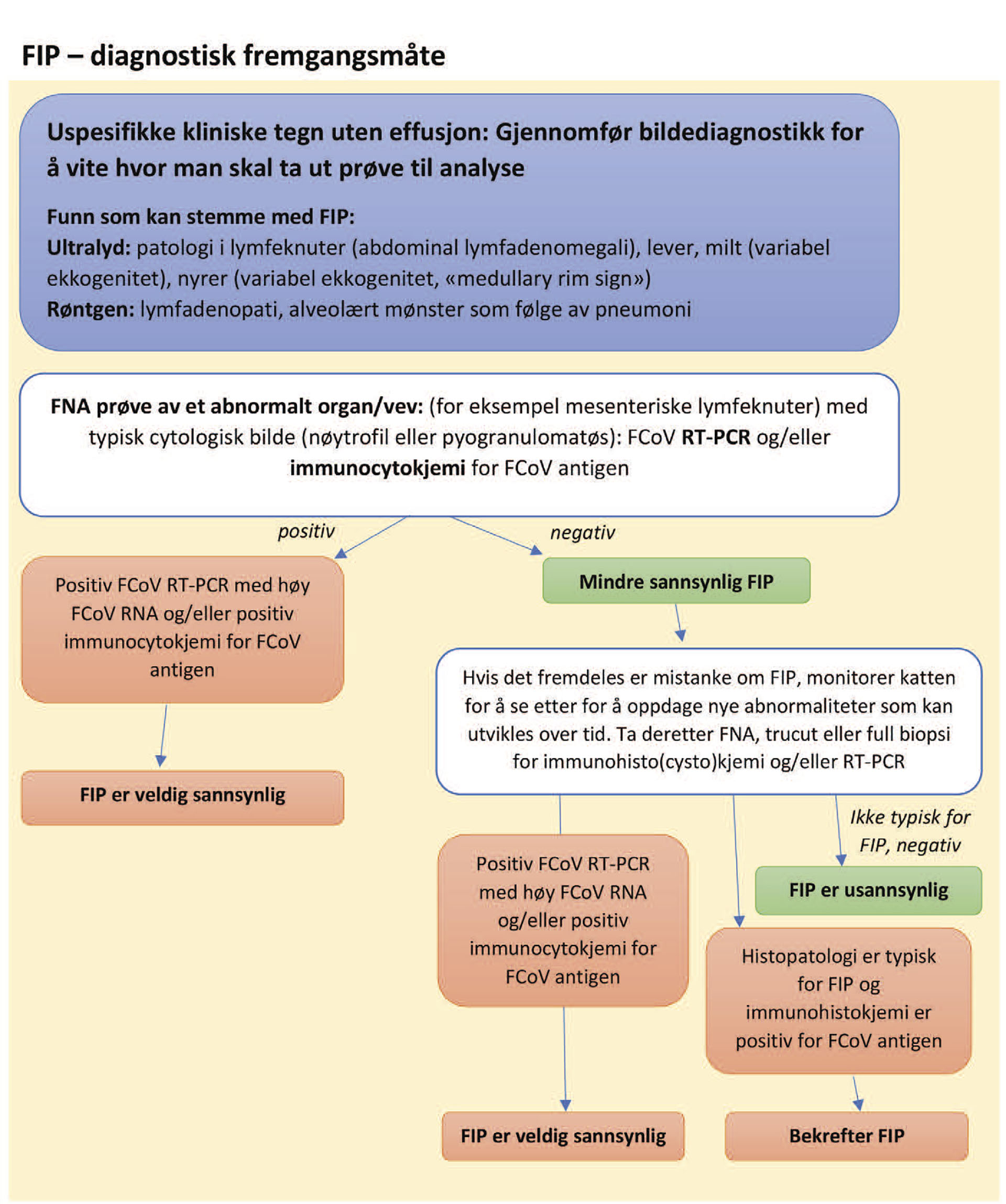
Figur 2: Diagnostisk fremgangsmåte ved mistanke om FIP uten effusjon. Figuren er hentet fra Tasker et al 2023, og oversatt til norsk (1).
Kasuistikker
Analyser i blod, serum og urin
For de to kasusene som presenteres ble hematologiske analyser utført med IDEXX ProCyte Dx®, standard biokjemisk serumanalyser ble utført med IDEXX Catalyst One® og urinundersøkelser ble uført med IDEXX VetLab® UATM Analyzer (IDEXX Laboratories, Inc. Westbrook, ME, USA) ved EMPET Stabekk AS. Analyser for FIP virus (FIP Virus RealPCRTM Test) og histologiske undersøkelser ble utført ved IDEXX referanselaboratorier eller Laboklin diagnostisk laboratorium i Tyskland.
Kasus 1
Signalement og anamnese
En 1,5 år gammel neva masquerade (maskefarget Sibirkatt), intakt hunnkatt kom til undersøkelse fordi eier hadde sett endring i atferd og noe nedsatt matlyst. De siste ukene hadde katten sluttet å leke, og var blitt aggressiv mot den andre katten i familien. I tillegg sov den mer, og eier synes katten virket lettere enn før. Katten var vaksinert, og behandlet med ormekur i henhold til anbefalinger. Den oppholdt seg kun innendørs, og hadde ikke vært i kontakt med andre katter enn den som bodde i samme hus. Sistnevnte viste ingen tegn på sykdom.
Klinisk undersøkelse
Katten var alert og responsiv, men hadde noe dårlig pelskvalitet og en BCS (Body Condition Score) på 3/9. Den hadde gått ned 200 g i vekt i løpet av 4 måneder og veide 2,8 kg. Ved palpasjon kunne det kjennes en distinkt fast, men mobil kul midt i buken. Øvrig klinisk undersøkelse var uten avvik.
Diagnostiske undersøkelser
Blod- og serumprøver viste moderat nonregenerativ anemi med en hematokrit på 21,8 %, og moderat hyperglobulinemi 55 g/L (28-51 g/L). Øvrige blod- og serumverdier var godt innenfor normale referanseintervall. Urinen hadde en spesifikk vekt på 1.040, uten signifikante funn på stix eller mikroskopi av sediment. Ved ultralyd ble det gjort funn av en hypoekkogen kul på 2,62x3,41cm i lengdesnitt, sentralt i kulen lå et større blodkar (Figur 3). Kulen lå midt i buken omgitt av fett og tynntarm. Små mengder fri væske ble observert. Et lite område langs kanten av venstre leverlapp hadde uregelmessig ekkogenitet, og ruglete overflate. Resten av leveren var uten påvisbare avvik ved ultralyd.
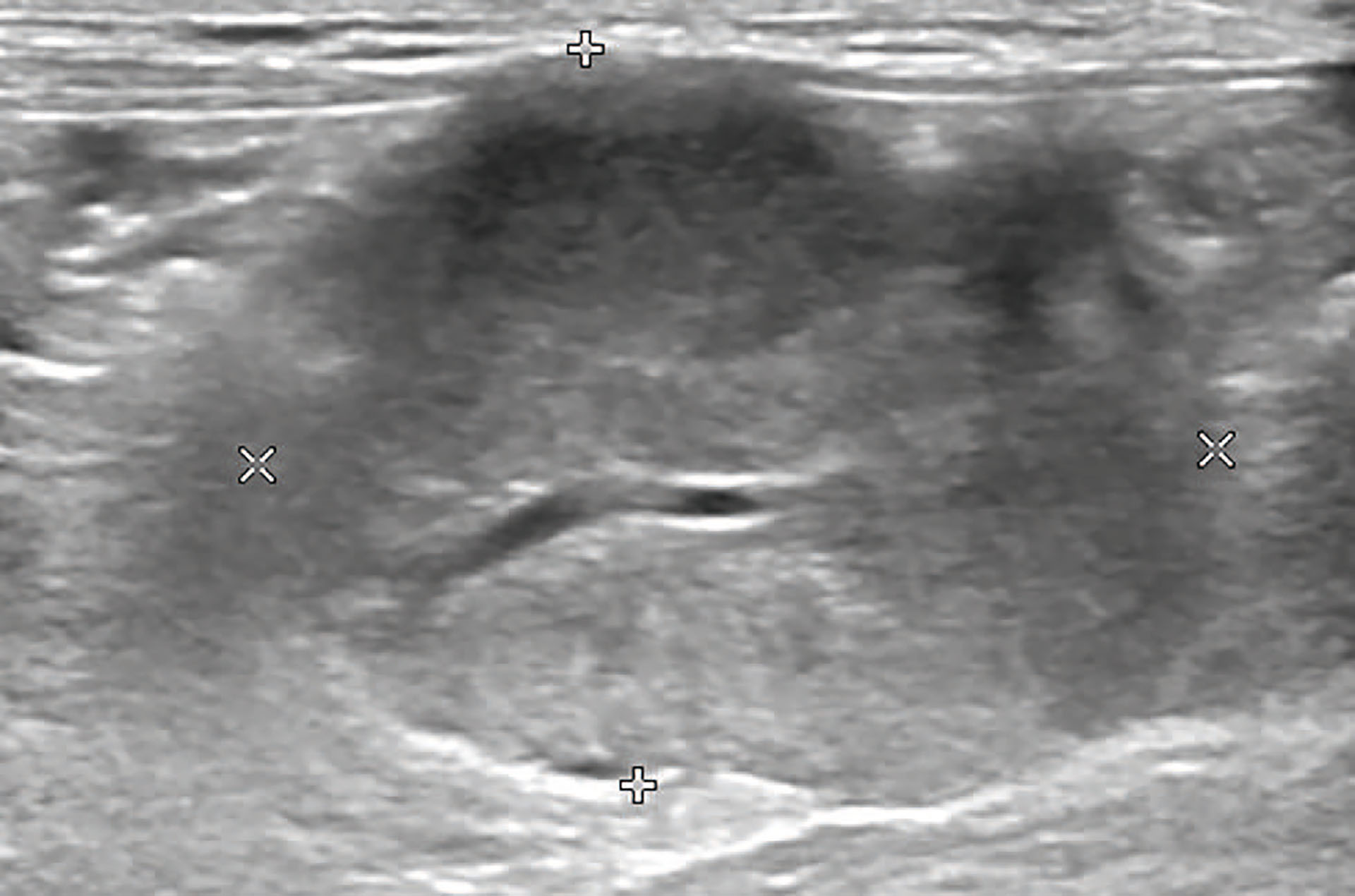
Figur 3: Ultralyd abdomen: Uregelmessig hypoekkogen kul i buken. Størrelse 2,62x3,41cm med et sentralt blodkar.
Foto: Sunniva Venås
Dagen etter første besøk ble katten lagt inn for eksplorativ laparotomi og prøvetaking av tumoren i buken. I forkant av operasjonen ble koagulasjonsparameterne APTT og PT målt, disse var innenfor normale referanseintervall. Saltvanns agglutinasjonstest (4 dråper NaCl blandet med 1 dråpe blod) ble også gjennomført uten tegn til agglutinasjon. Blodutstryk ble undersøkt uten funn av blodparasitter.
Under operasjonen ble kulen lokalisert med ultralyd i tarmkrøset med diameter 3-4 cm. Leveren var i tillegg gjennomsatt med hvite små kuler. Det ble først tatt prøve av den frie væsken, deretter vevsprøver fra både kulen i tarmkrøset og leveren.
Vevsprøvene fra kulen og leveren viste en alvorlig granulomatøs/pyogranulomatøs inflammasjon med nekrotiske foci og fibrose. Histologisk snitt fra kulen i tarmkrøset er vist i Figur 4. Det var ingen tegn til neoplastiske celler eller parasitter. Både PAS (Periodic Acid Schiff)-farging for påvisning av sopp og modifisert Ziehl-Neelsen farging for påvisning av syrefaste bakterier var negative. Ascitesvæsken ble analysert med kvantitativ FCoV RT-PCR og var positiv.
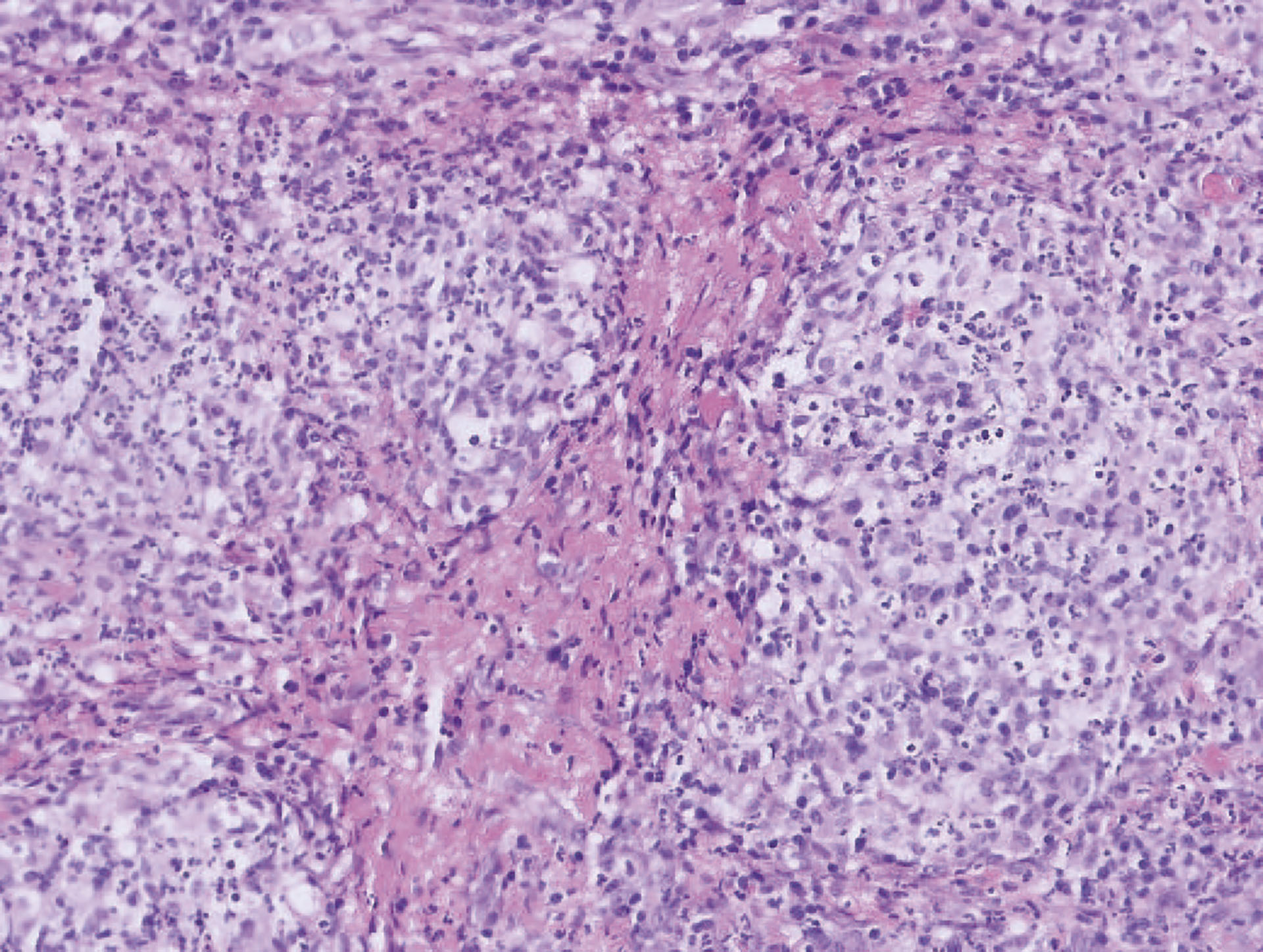
Figur 4: Pyogranulomatøs inflammasjon med fibrose fra kulen i tarmkrøset.
Foto: IDEXX referanselaboratorium, Tyskland
Tentativ diagnose
FIP basert på kliniske funn, histologiske funn og positiv FCoV RT-PCR i ascitesvæsken.
Behandling
Behandling ble igangsatt med 37,5 mg GS-441524 (¾ 50 mg tablett) SID i 12 uker. Anbefalt dose er 10-12 mg/kg (1,8). Det ble lagt opp plan for monitorering med blodprøve etter to uker, deretter hver måned. Kastrasjon ble anbefalt når katten var blitt klinisk frisk for å redusere stress i forbindelse med løpetid.
Videre oppfølging og konklusjon

Figur 5: Frisk katt etter behandling mot FIP (Kasus 1).
Foto: Eier
Eier ble kontaktet en uke etter igangsatt behandling. Katten var nå i full vigør, spiste normalt, var aktiv og lekte med den andre katten igjen.
Ved neste kontroll to uker etter igangsatt behandling kunne kulen fremdeles palperes i buken. Katten virket livlig og hadde bedre pelskvalitet. Hematologiske analyser viste normalisering av anemien med en hematokrit på 36,2 %. Biokjemisk serumanalyse viste fremdeles mild hyperglobulinemi på 53 g/L (28-51 g/L).
Ved neste kontroll 6 uker etter igangsatt behandling kunne eier fortelle at katten hadde hatt flere løpetider, virket stresset og spiste mindre. Katten hadde gått ytterligere 200 g ned i vekt. Blodprøvene var nå uten avvik. Katten ble kastrert samme dag.
Katten kom inn for kontroll 10 dager etter kastrasjonen. Vekten hadde økt med 170 g, og operasjonssåret hadde grodd fint. Ved bukpalpasjon kunne kulen ikke kjennes. Det ble avtalt å ta kontrollblodprøver etter behandlingsslutt.
Ved siste kontroll 16 uker etter behandlingsstart hadde katten (Figur 5) gått opp 1 kg i vekt og blodprøvene var uten avvik. Ved rutinemessig vaksineinnkalling fem måneder etter endt kur viste katten ingen tegn på tilbakefall.
Kasus 2
Signalement og anamnese
En ett år gammel kastrert hunnkatt, blandingsrase, ankom klinikken etter å ha kommet hjem fra kennelopphold tre uker tidligere. Eier hadde merket endret atferd, og ustelt pels med avføring. Katten sov mye, virket nedstemt og slapp, og ville ikke leke eller gå ut. Eier merket at katten var mindre interessert i mat etter kenneloppholdet. Katten hadde vært i Norge siden den ble født, ble sterilisert ved sju måneders alder og var vaksinert og behandlet med ormekur i henhold til anbefalinger.
Klinisk undersøkelse
Katten var nedstemt, men alert og responsiv. Den var dårlig muskelsatt, veide 3,3 kg, og hadde BCS på 3/9. Katten viste tegn til dehydrering med stående hudfold på 1 sek. Ved palpasjon av buk kjentes den myk ut, med en viss distensjon. Katten hadde feber med rektal temperatur på 40,3 °C.
Diagnostiske undersøkelser
Blodprøver ble analysert på klinikklaboratoriet og hematologiske analyser viste mild non-regenerativ anemi (hematokrit på 28,2 %), nøytrofili og eosinopeni. Blodutstryk viste kraftig rouleaux-dannelse av de røde blodcellene. Biokjemiske analyser av serum viste hyperglobulinemi på 61 g/L (28-51 g/L) og hyperbili-rubenemia på 19 mmol/L (0-15 mmol/L). Albumin/globulin ratio var 0,4. FIV/FeLV snap-test var negativ. Det ble utført ultralyd av buk hvor det ble funnet fri væske, mesenterisk lymfadenopati og generelt fortykkede vegger i fordøyelsessystemet (Figur 6).
Væsken tatt ved abdominocentese var gul og trådtrekkende. Refraktometer viste totalprotein på 65 g/L. Ascitesvæsken ble analysert med kvantitativ FCoV RT-PCR og var positiv for FCoV-RNA, og positiv for Mutation M1058L.
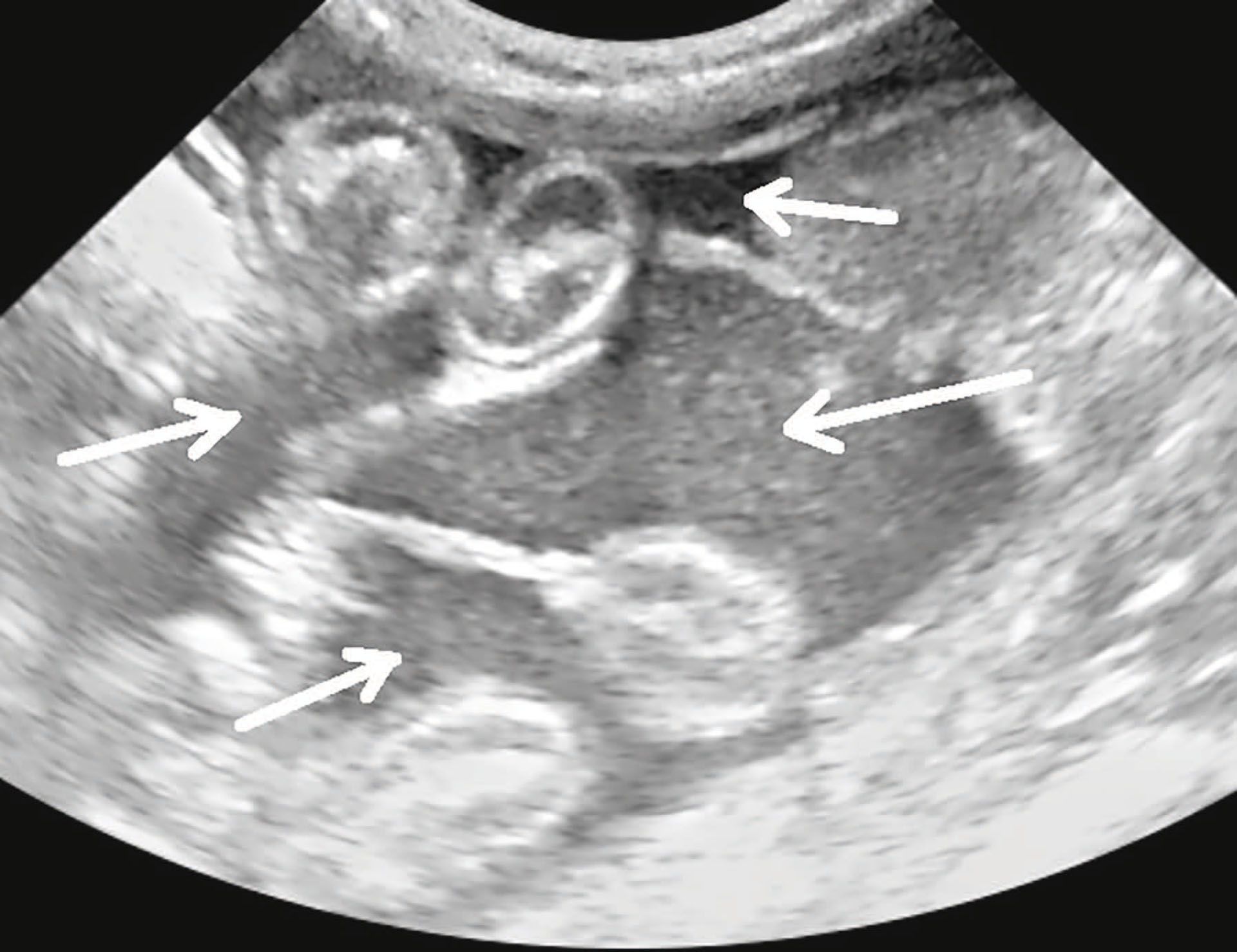
Figur 6: Ultralyd viste fri væske i buk (Piler).
Foto: Sunniva Venås
Tentativ diagnose
«Våt FIP» basert på anamnese, kliniske og diagnostiske undersøkelser med positiv FCoV-RNA og funn av mutasjon M1058L i ascitesvæske.
Behandling
Katten ble først gitt væskebehandling med RingerAcetat iv, 10 mL/kg/t i 2 timer for rehydrering, deretter redusert til 5 mL/kg/time, totalt 116 mL. GS-441524 50 mg tabletter ble bestilt som ankom klinikken to dager senere. Katten ble gitt ¾ tablett SID etter anbefalt dose (10-12 mg/kg SID). Medisineringen ble planlagt å vare i 12 uker, med kontroll to uker etter behandlingsstart og deretter månedlig.
Videre oppfølging og konklusjon
Allerede to dager etter oppstart av medisineringen informerte eier at katten hadde respondert på behandlingen, den virket kvikkere og mer våken. To uker senere var katten inne for kontroll på klinikken. Eier oppfattet katten som sitt «gamle jeg» igjen, mer energisk og leken. Appetitten var nå normal, og katten hadde gått opp 450 gram i vekt. Hematologiske analyser viste fremdeles non-regenerativ anemi (hematokrit 28,4 %), men ingen avvik for leukocyttene. Hyperglobulinemien hadde økt ytterligere til 63 g/L, og albumin/globulin ratio var på 0,4. Det ble likevel vurdert som god respons på behandling da katten var klinisk mye friskere enn for to uker siden og den hadde gått opp i vekt. Globuliner har lang halveringstid og en økning oppstår hvis mye effusjon absorberes. Fordi ascitesvæsken kan bli absorbert på kort tid, vil også noen ganger en ytterligere reduksjon i hematokrit de første ukene etter behandlingsstart kunne oppleves. Denne type endring i blodverdier er ikke forbundet med dårlig respons på behandling (1,8).
Ved kontroll syv uker etter oppstart av behandling hadde kattens vekt økt ytterligere med 450 gram. Ifølge eier var katten helt seg selv, med et meget høyt energinivå. Hematologiske analyser var uten avvik. Globulinene var redusert til 47 g/L (innenfor referanseintervallet), og albumin-globulin ratio hadde økt til 0,6. Planen videre ble å fortsette medisineringen uendret. Neste kontroll ble avtalt på dag 84 etter behandlingsstart.
På siste og avsluttende kontroll hadde katten respondert svært godt på behandling. Vekten var økt med 1,2 kg og eier opplevde katten som helt frisk. Blod- og serumanalyser var uten avvik, totalprotein var nå på 69 g/L, albumin 28 g/L, globuliner 41 g/L, som ga en albumin/globulin ratio på 0,7. Abdominal ultralyd ble utført, og det var ikke lenger tegn til ascites eller lymfadenopati. Katten ble erklært frisk og behandlingen avsluttet. Ved rutinemessig vaksinering tre måneder etter endt kur viste katten ingen tegn på tilbakefall.
Diskusjon
Prognosen for FIP er tidligere angitt å være ekstremt dårlig (2). I senere tid har interessen rundt behandlingen av koronavirus økt betraktelig, og forskning har endelig gitt resultater.
RemdesivirTM eller GS-5734 (Gilead Scienses Inc., Foster City, CA, USA) er forløperen til metabolitten GS-441524 (Gilead Sciences, Inc., Foster City, CA, USA), en RNA-polymerasehemmer (Figur 7). Remdesivir (Veklury®, Gilead Sciences Nordic, pulver til infusjonsvæske 100 mg) brukes i behandlingen av pasienter infisert med covid-19. Veklury® kan også bestilles til dyr, men er kun holdbar i 48 timer i kjøleskap etter anbrudd. Medisinen er kun aktuell som innledende behandling grunnet lokal smertereaksjon ved injeksjonsstedet (1,4). GS-441524 finnes nå som tabletter, og kan tas inn på registreringsfritak til katt. Tablettene er tilsatt tunfisksmak og kan til nød knuses og gis sammen med litt våtfôr.
Remdesivir ble først testet på pasienter smittet med ebolavirus, et RNA-virus i familien Filoviridae. Siden medisinen viste lovende resultater for RNA-virus som ebolavirus og koronaviruset SARS-CoV-2 var det ønskelig å teste ut om det hadde samme effekt mot viruset som forårsaker FIP (5,6).
I april 2023 fikk VESO importtillatelse for GS-441524 tabletter fra legemiddelselskapet Bova i Storbritannia som nå er tilgjengelig på godkjenningsfritak. Tablettene (50 mg), er små og kan deles i fire. Doseringsprotokoller og anbefalinger for oppfølging er blant annet publisert i Journal of Feline Medicine and Surgery (7), hos International Cat Care (8) og av European Advisory Board on Cat Diseases (1). Dosering av GS-441524 er 10-15 mg/kg SID i 12 uker (1,8). I enkelte studier har høyere doser (15-20 mg/kg SID) blitt brukt til katter med tilbakefall (9,10). Til å begynne med ble kattene behandlet med remdesivir eller GS-441524 i injeksjonsform. Så kom protokoller med injeksjonsbehandling i oppstartsfasen etterfulgt av peroral medisinering. GS-441524 tablettene ser heldigvis ut til å gi like gode resultater som injeksjonsbehandling så lenge katten ikke er for syk for peroral administrering (1,8,9,13). Da GS-441524 først kom ble kattene behandlet med en mye lavere dose (6,11). I en studie ble det benyttet subkutan injeksjon med GS-441524 med en dose på mellom 2 til 5 mg/kg i 14 dager (11). To av ti katter hadde tilbakefall, men disse responderte på ny behandling, og 8 måneder senere var alle normale. I en annen studie ble det behandlet 31 katter med GS-441524 dosert 2 mg/kg sc. SID i 12 uker (6). Fire av kattene døde eller ble avlivet to til fem dager etter oppstart grunnet alvorlig sykdom og 1 katt ble avlivet etter 26 dager på grunn av manglende respons på behandling. De resterende 26 kattene gjennomførte minst 12 uker med behandling. Tilbakefall oppstod hos åtte katter, og disse ble på ny behandlet med samme eller høyere dose (4 mg/kg). En av kattene som fikk samme dose som før hadde nevrologisk FIP og døde senere på grunn av et nytt tilbakefall. De andre syv kattene responderte bra og forble friske (6). Injeksjon med GS-441524 svir, heldigvis viser det seg at peroral behandling med tabletter også har god effekt mot FIP. I en større studie med 324 katter ble 81 % behandlet med tabletter, 7,5 til 10 mg/kg i 12 uker. Av kattene med kombinert våt og tørr FIP ble 85 % friske, og blant kattene med våt FIP ble 94 % friske (12). Nevrologisk FIP er forbundet med dårligere prognose (1). The International Society of Feline Medicine har lagt ut en oppdatert behandlingsanbefaling (8) (Se faktaboks).
Ukastrerte katter bør kastreres når de er klinisk friske og helst 4 uker før behandlingen avsluttes. Stress i forbindelse med løpetid kan øke risiko for tilbakefall. Tiltak for å redusere stress hjemme (for eksempel redusere antall katter i huset) og på klinikken (minst mulig hospitalisering) anbefales (8).
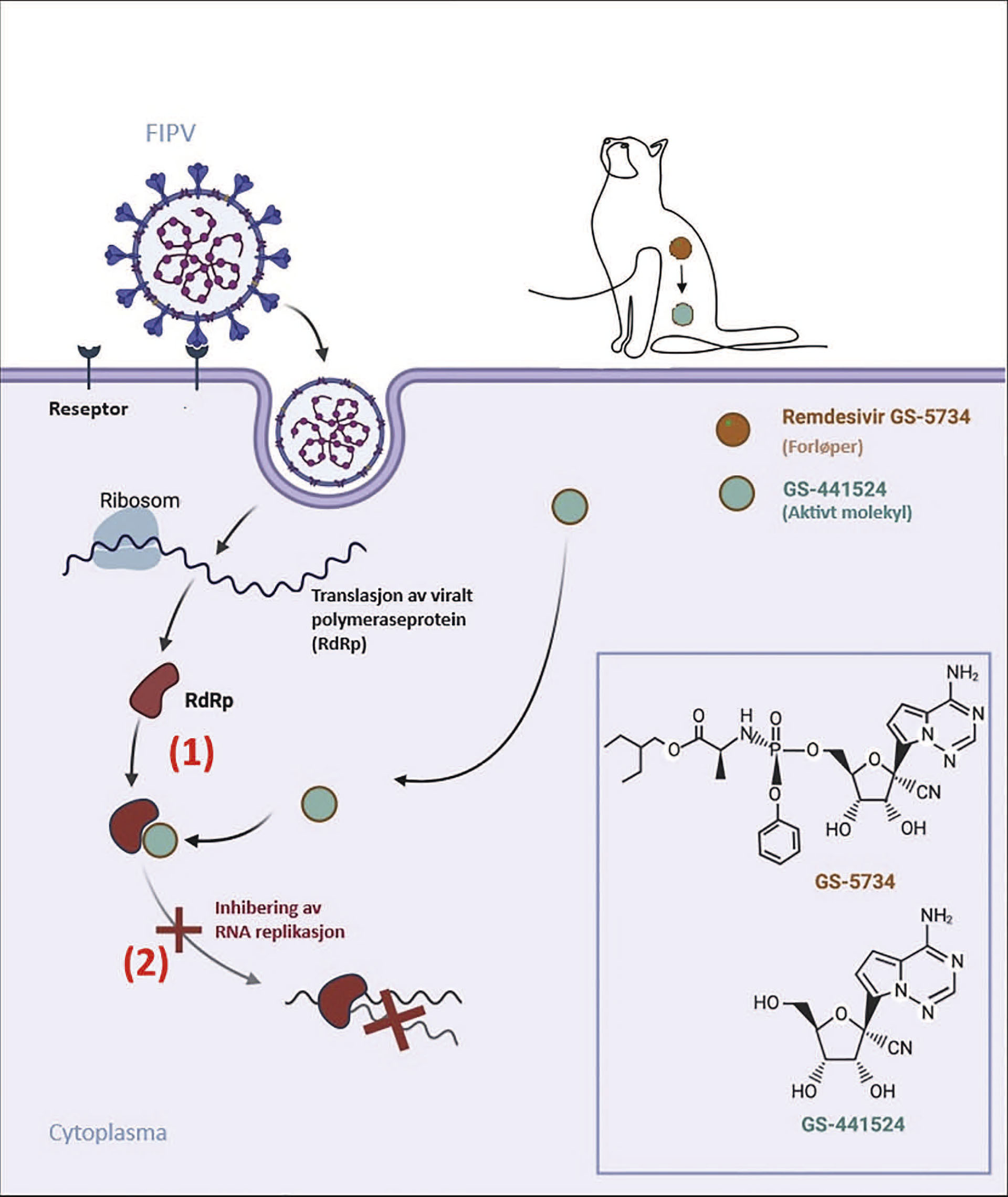
Figur 7. Virkningsmekanismen til GS-441524.
(1). GS-441524 er strukturelt likt adenosin, en av byggesteinene i RNA. Når viruset replikerer sitt RNA-genom ved hjelp av virusindusert polymeraseprotein (RdRp), inkorporeres GS-441524 i den voksende RNA-kjeden i stedet for adenosin. GS-44152 skader i liten grad vertens RNA fordi det er mer selektivt for den virale RNA-polymerasen.
(2). Når GS-441524 er inkorporert i viralt RNA inhiberer det RNA-replikasjonen som resulterer i et ikke-fungerende viralt RNA.
Figuren er hentet fra Frediansyah et al., og tilpasset denne artikkelen (5).
Doseringsanbefaling for GS-441524 tabletter (8):
«Tørr» eller «våt» FIP uten nevrologiske tegn: 10-12 mg/kg SID i 12 uker
FIP med oftalmologiske tegn: 15 mg/kg SID i 12 uker
FIP med nevrologiske tegn: 10 mg/kg BID i 12 uker
Dersom det fremdeles er effusjon ved to ukers kontroll, er det anbefalt å øke dosen med 3-5 mg/kg.
Bivirkninger av GS-441524
Rapporterte bivirkninger av GS-441524 i tablettform har heldigvis virket å være færre enn for injeksjonsformen av remdesivir. En mild økning av ALT er rapportert, men det er usikkert om dette er grunnet sykdom eller medisin (1,8,13). En mild økning i ALT ble sett hos kasus 2 (ALT på 22 U/L ved diagnosetidspunkt, 58 U/L to uker etter oppstart medisinering og 59 U/L syv uker etter oppstart medisinering). Det er også rapportert om lymfocyttose og eosinofili som bivirkning (1,13)..
Kostnader ved diagnostikk og behandling av FIP
Det er anbefalt kontroll to uker etter oppstart med GS-441524, og deretter månedlig til behandlingen med GS-441524 avsluttes. I forbindelse med disse kontrollene er det anbefalt både biokjemiske og hematologiske analyser og ultralyd etter avsluttet behandling (8). Blodprøvene i forbindelse med kontrollene tas for å monitorere progresjon. Dersom katten viser tydelig klinisk bedring, kan antall blodprøver etter behandlingsstart reduseres. Medisinkostnaden for 10 tabletter (50 mg per tablett) GS-441524 fra VESO er 4602,50 NOK inkludert MVA (februar 2024), og 20 tabletter koster 7866,25 NOK (februar 2024). En katt på rundt 3 kg trenger ¾ tablett daglig, og vil i løpet av 84 dager trenge 63 tabletter. Medisinkostnaden for GS-441524 for eier (beregnet på 3 kg katt) blir på minst 28.000 NOK inkludert mva.
Selv om det foreløpig ikke foreligger langtidsstudier kan det se ut til at behandlingen med GS-441524 er kurativ for FIP. Respons på behandling ses allerede de første dagene etter oppstart, så en mulig løsning er at eier kjøper de første tablettene ved klinikken for å se om katten responderer før de kjøper hele pakken fra apoteket. En flaske med remdesivir (Veklury®) koster 5293,40 NOK (februar 2024) og er nok for to dagers behandling av en katt på 5 kg. For å følge legemiddelkaskaden skal man velge Veklury® fremfor tablettene, men siden behandlingslengden er 12 uker er ikke dette et aktuelt alternativ. Smerte som følge av injeksjonene er en vanlig bivirkning, og det blir for mange eiere umulig å injisere katten på sikt (8). I tillegg vil prisen på 84 dagers behandling ligge på godt over 200 000 NOK.
Konklusjon
FIP er en sykdom de aller fleste praktiserende smådyrveterinærer møter. Medisinen GS-441524 er nyutviklet mot en sykdom som ubehandlet er en dødsdom. Ingen medisin har tidligere vært i nærheten av å gi de samme resultatene mot FIP. Forfatterne av denne artikkelen har i løpet av sommeren 2023 behandlet to pasienter med GS-441525. Begge ble betydelig friskere i løpet av noen dager. Medisinen er kostbar, men den har vært enkel å administrere for eierne, og har få bivirkninger. På grunn av den raske effekten er det aktuelt å starte opp medisineringen i påvente av prøvesvar dersom det er sterk klinisk mistanke. Både dose og lengde på behandlingen kan bli endret etter hvert som medisinen blir utprøvd. Det kan tenkes at en høyere dose kan korte ned behandlingslengden. Det er interessant å følge med på behandlingsresponsen ved hjelp av blodprøver og bildediagnostikk, men det trenger ikke være et kriterium for å begynne medisineringen.
Sammendrag
Felin infeksiøs peritonitt (FIP) er forårsaket av infeksjon med kattens koronavirus (FCoV), et enkeltstrenget RNA-virus. FIP har inntil nylig blitt regnet som 100 % dødelig. I kjølvannet av covid-19-pandemien, er det utviklet nye antivirale medisiner mot infeksjon med koronavirus. En av disse, GS-441524, er en adenosinanalog som kan terminere virusreplikeringen hos katter med FIP. I artikkelen presenteres to katter som har blitt behandlet med GS-441524. Begge kattene responderte meget raskt, og de restituerte fullstendig i løpet av behandlingstiden som er anbefalt til 12 uker.
Summary
Feline Infectious Peritonitis (FIP) is caused by infection with Feline Coronavirus (FCoV), a single-stranded RNA virus. FIP has, until recently, been considered 100 % fatal. In the wake of the COVID-19-pandemic, new antiviral medications have been developed for coronavirus infections. One of these, GS-441524, is an adenosine analog that can terminate virus replication in cats with FIP. The article describes two cats that have been treated with GS-441524. Both cats responded very quickly, and they fully recovered during the recommended 12-week treatment period.
Referanser
Tasker S, Addie DD, Egberink H, Hofmann-Lehmann R, Hosie MJ, Truyen U et al. Feline infectious peritonitis: European Advisory Board on Cat Diseases Guidelines. Viruses 2023;15:1847.
Hartmann K. Coronavirus infections (canine and feline), including feline infectious peritonitis. I: Ettinger SJ, Feldman EC, Côté E, eds. Textbook of veterinary internal medicine: diseases of the dog and cat. 8th ed. St. Louis, Missouri: Saunders Elsevier, 2017:983-91.
Riemer F, Kuehner KA, Ritz S, Sauter-Louis C, Hartmann K. Clinical and laboratory features of cats with feline infectious peritonitis: a retrospective study of 231 confirmed cases (2000–2010). J Feline Med Surg 2016;18:348–56.
Veklury. I: Felleskatalogen. https://www.felleskatalogen.no/medisin/veklury-gilead-677450 (06.04.2024).
Frediansyah A, Nainu F, Dhama K, Mudatsir M, Harapan H. Remdesivir and its antiviral activity against COVID-19: a systematic review. Clin Epidemiol Glob Health 2021;9:123–7.
Pedersen NC, Perron M, Bannasch M, Montgomery E, Murakami E, Liepnieks M et al. Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis. J Feline Med Surg 2019;21:271–81.
Thayer V, Gogolski S, Felten S, Hartmann K, Kennedy M, Olah GA. 2022 AAFP/Every cat feline infectious peritonitis diagnosis guidelines. J Feline Med Surg 2022;24:905–33.
Taylor S, Tasker S, Gunn-Moore D, Barker E, Sorrell S. An update on treatment of FIP in the UK. The International Society of Feline Medicine 2023. https://icatcare.org/app/uploads/2023/03/An-update-on-treatment-of-FIP-in-the-UK-2023.pdf (06.04.2024).
Coggins SJ, Norris JM, Malik R, Govendir M, Hall EJ, Kimble B et al. Outcomes of treatment of cats with feline infectious peritonitis using parenterally administered remdesivir, with or without transition to orally administered GS-441524. J Vet Intern Med 2023;37:1772–83.
Zwicklbauer K, Krentz D, Bergmann M, Felten S, Dorsch R, Fischer A, et al. Long-term follow-up of cats in complete remission after treatment of feline infectious peritonitis with oral GS-441524. J Feline Med Surg 2023;25:1098612X231183250.
Murphy BG, Perron M, Murakami E, Bauer K, Park Y, Eckstrand C et al. The nucleoside analog GS-441524 strongly inhibits feline infectious peritonitis (FIP) virus in tissue culture and experimental cat infection studies. Vet Microbiol 2018;219:226–33.
Katayama M, Uemura Y. Prognostic prediction for therapeutic effects of Mutian on 324 client-owned cats with feline infectious peritonitis based on clinical laboratory indicators and physical signs. Vet Sci 2023;10:136.
Krentz D, Zenger K, Alberer M, Felten S, Bergmann M, Dorsch R et al. Curing cats with feline infectious peritonitis with an oral multi-component drug containing GS-441524. Viruses 2021;13:2228.