Her er diagnosen! Perianalkjerteladenom i preputium
AniCura Jeløy Dyresykehus
Cytologisk undersøkelse
Det ble undersøkt til sammen syv utstryk som var farget med en modifisert Wright’s metode (Hematek Siemens). I fire av disse var det sparsomt med materiale som vesentlig bestod av blod. I de tre andre var det rikelig med materiale med god utstrykskvalitet. Det ble påvist en rosa bakgrunn og et høyt antall erytrocytter og blodplater i små klumper, forenlig med inngrepsblødning. Det var et høyt til svært høyt antall kjerneholdige celler av samme type som fantes i små og store, tidvis tette, klumper og flak (Figur 4). Cellene hadde en lav til moderat kjerne til cytoplasma (n/c) ratio og et granulert, blårosa cytoplasma. Sentralt i cellene fantes en rund kjerne med finstiplet kromatin og ofte en liten til moderat stor sentral nukleole. Det var mild anisokaryose (Figur 5).
Cytologisk diagnose
De cytologiske funnene var forenlig med en epitelial neoplasi, perianalkjerteltumor; sannsynligvis et perianalkjerteladenom («hepatoid» adenom).
Et veldifferensiert adenokarsinom ble ansett som mindre sannsynlig, både basert på cytologiske funn og kunnskap om at de er langt sjeldnere forekommende hos hund. Histologisk undersøkelse er imidlertid nødvendig for sikrere å kunne skille mellom disse diagnosene.
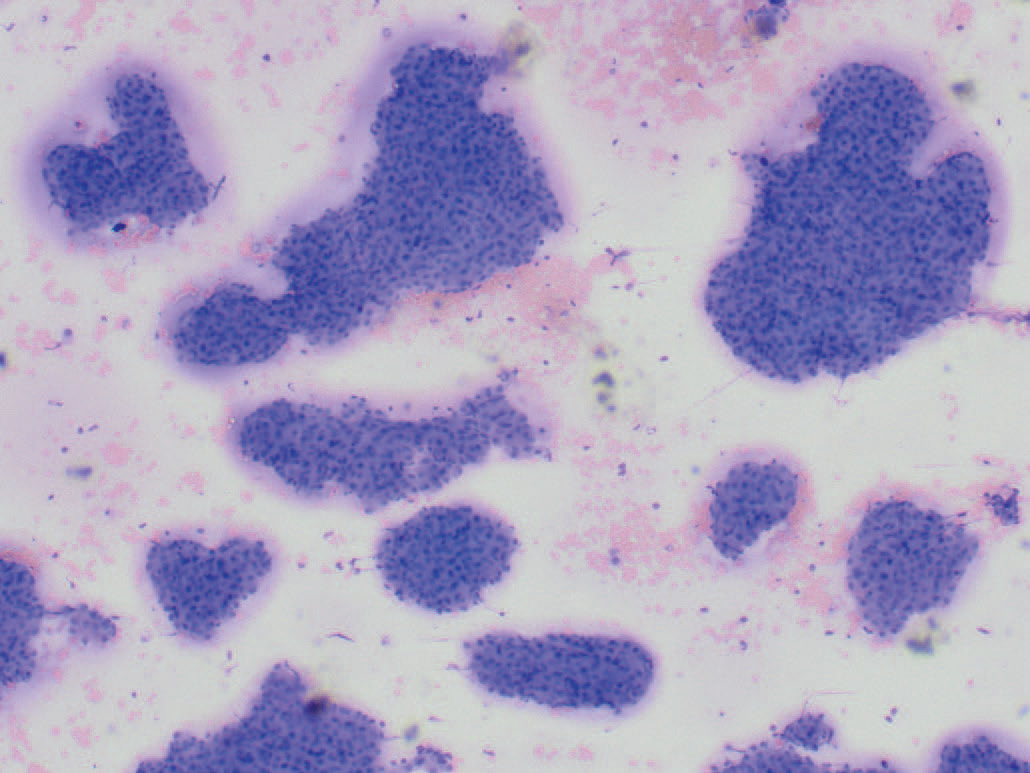
Figur 4. Rosa bakgrunn med mange erytrocytter og et høyt til svært høyt antall kjerneholdige celler av samme type som fantes i små og store klumper og flak. Modifisert Wright’s farging. Objektiv 4x. Foto: Bente Kristin Sævik
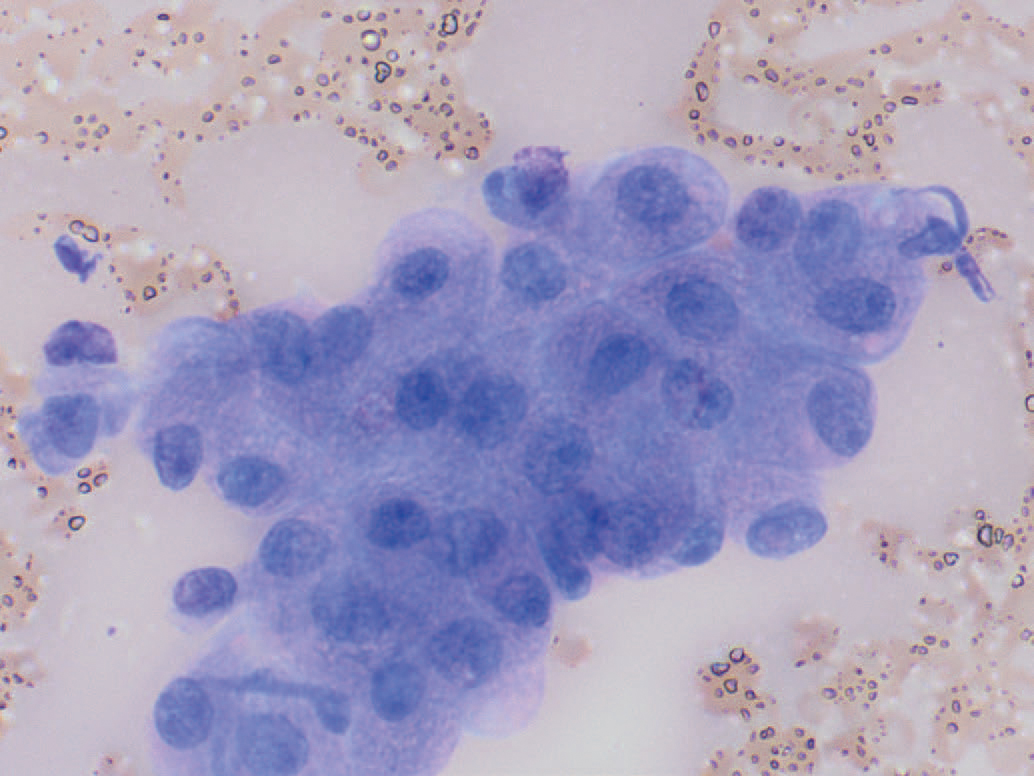
Figur 5. Cellene hadde en lav til moderat kjerne til cytoplasma (n/c) ratio og et granulert, blårosa cytoplasma. Sentralt i cellene fantes en rund kjerne med finstiplet kromatin og ofte en liten til moderat stor sentral nukleole. Det var mild variasjon i kjernestørrelse (anisokaryose). Modifisert Wright’s farging. Objektiv 40x. Foto: Bente Kristin Sævik
Kirurgisk behandling
En mulig effekt av kastrasjon på massens størrelse (reduksjon eller remisjon) ble diskutert med eier, men eier ønsket ikke å kastrere hunden. Det ble bestemt å fjerne massen med frie, men ikke utvidede marginer og med påfølgende histologisk undersøkelse.
Hunden ble premedisinert med acepromazin 0,05 mg/kg (Plegicil® vet, 10 mg/mL, Pharmaxim AB) kombinert med metadonhydroklorid 0,5 mg/kg i.m. (Synthadon® vet, 10 mg/mL, Le Vet) i tillegg til robenakoksib 2 mg/kg s.c. (Onsior®, 20 mg/mL, Elanco).
Anestesi ble indusert med propofol 4 mg/kg i.v. (PropoVet®), Zoetis, 10 mg/ml) og hunden ble intubert. Generell anestesi ble vedlikeholdt med en blanding av 100 % oksygen og 2 % sevofluran (SevoFlo®, Zoetis) og hunden ble klargjort for aseptisk kirurgi. Lokal anestesi ble gitt i form av lidokainhydroklorid 2 mg/kg s.c. (Xylocain®, 10 mg/mL, Aspen Pharma Trading Ltd.).
Området ble standard dobbelt-tildekket og massen ble fjernet etter premarkerte linjer tilsvarende marginer på 1 cm kranialt, kaudalt, medialt og lateralt og et fascialtplan dypt. Marginene ble markert med en steril penn (Viomedex Ltd.). Hjørner samt dybde på massen ble markert med 3-0 PDS (polydioxanone) sutur og sendt for histologisk undersøkelse (Figur 6).
Kirurgiske instrumenter, samt tildekning, ble byttet før innsnittet ble lukket med en «advancement flap». Flapen ble suturert med Polygalactin 910 3-0 (Vicryl, Ethicon) i underhuden og Polyamid 3-0 (Supramid, Braun) i huden (Figur 7). Inngrepet forløp uten komplikasjoner, og under hele inngrepet og inntil den var våken fikk hunden Ringer-acetat 4 mL/kg i.v. (Fresenius Kabi).
Hunden ble hospitaliserti 24 timer for observasjon og analgetisk behandling med Metadonhydroklorid 0,3 mg/kg i.m. (Synthadon® vet, 10 mg/mL, Le Vet,) hver fjerde time med start fra premedisinering og observasjon. Hunden ble sendt hjem med instruksjon til eier om kun korte lufteturer i bånd de første 14 dagene, samt med en resept på robenakoksib 2 mg/kg p.o. SID (Onsior®, 20 mg tabletter, Elanco). En Buster halskrage ble brukt for å forhindre slikking og biting i operasjonsområdet.
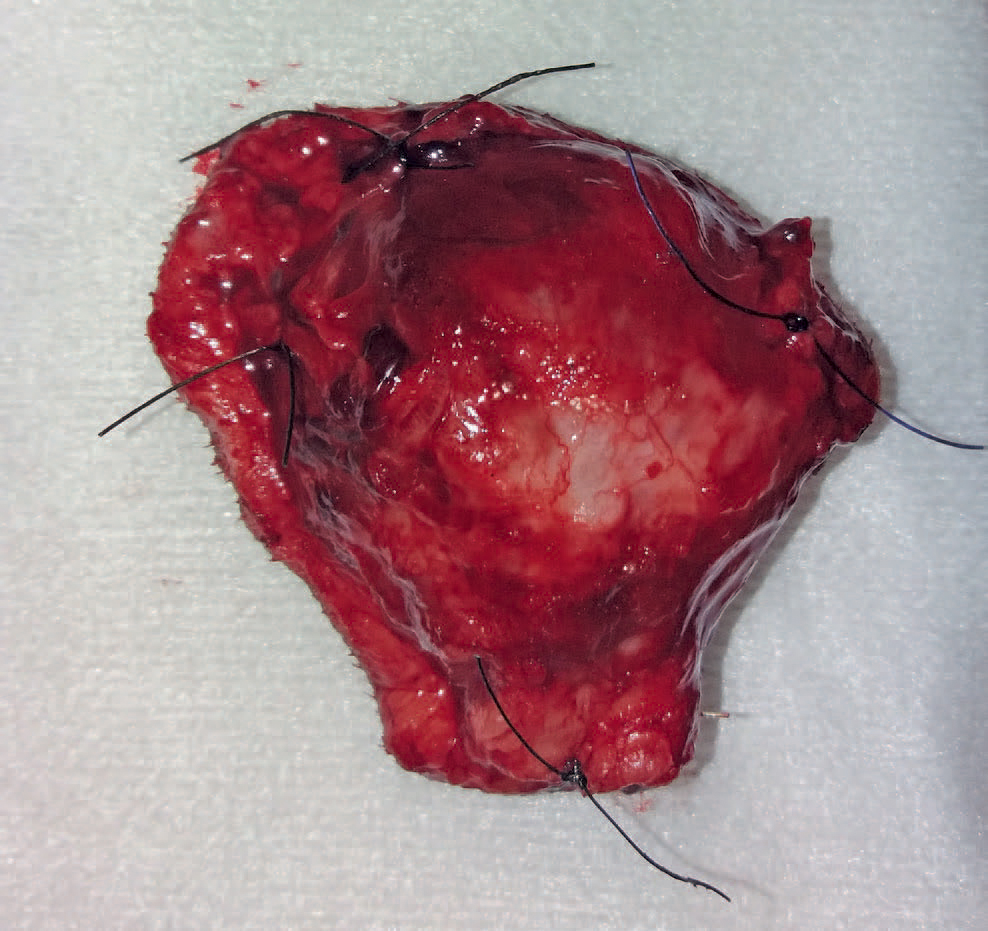
Figur 6. Massen etter fjerning, merket med sutur for å sikre adekvat orientering ved histologisk undersøkelse. Foto: Jon Andre Berg
Postoperativ kontroll og histologisk diagnose
Den postoperative perioden forløp uten nevneverdige problemer og 14 dager etter inngrepet var hunden tilbake i klinikken for fjerning av stingene. Såret hadde helet uten komplikasjoner.
Den histologiske diagnosen ble perianalkjerteladenom. Massen var fjernet med små, men frie marginer. Eier ble instruert i å sjekke hundens hud regelmessig med henblikk på opptreden av nye masser og igjen ta kontakt med veterinær i så tilfelle.
Diskusjon
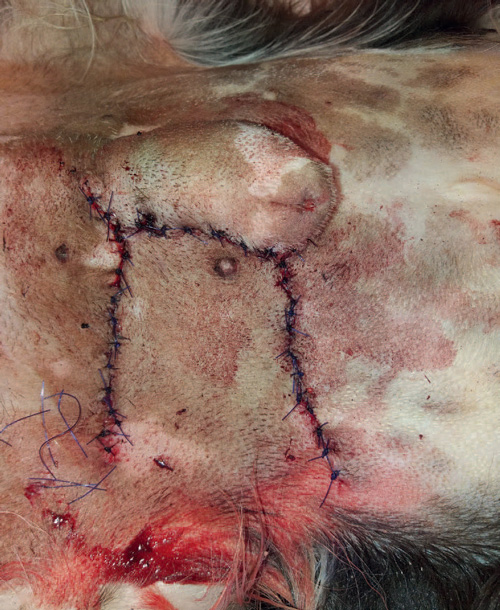
Figur 7. Flapen, som ble brukt til å dekke sårhulen, etter at den er suturert fast. Foto: Jon Andre Berg
En høy andel neoplasier hos hund er lokalisert til huden. Mange er benigne og diagnosen stilles vanligvis ved hjelp av cytologisk eller histologisk undersøkelse (1). Perianalkjertlene er modifiserte sebaceøse kjertler som vesentlig finnes rundt anus. Et lavt antall er også lokalisert i huden på halen, preputium, lår og rygg. Tre typer perianalkjerteltumorer er beskrevet; adenomer, adenokarsinomer og en perianalkjerteltumor som utelukkende består av reserveceller (små celler med høy n/c ratio) og som kalles perianalkjertelepiteliom (2, 3).
Perianalkjerteladenomer er vanligst hos eldre, intakte hannhunder, men kan også opptre hos tisper (primært kastrerte) og kastrerte hanndyr. De opptrer hyppigst i den ikke-behårede huden perianalt og de kan ulcerere og eventuelt bli infiserte. Overhyppigheten hos hannhunder er forklart ved at tumorcellene har reseptorer for androgener og kastrasjon vil derfor føre til regresjon eller kurasjon av de fleste benigne perianalkjerteltumorer. Disse metastaserer heller ikke, slik at stadiumbestemmelse («staging») er ikke nødvendig.
Perianalkjerteladenokarsinomer er langt sjeldnere og opptrer hos eldre hunder, både tisper, hannhunder og kastrerte individer. Disse vokser ofte raskt, ulcererer og er adherente til underliggende vev. Etter kirurgisk fjerning vil de kunne residivere. På diagnosetidspunktet er imidlertid forekomsten av metastaser lav (2-4).
Andre neoplasier som opptrer perianalt er analsekkadenokarsinomer («Apocrine gland anal sac adenocarsinomas»/AGASACAs). Disse opptrer sjeldnere enn perianalkjerteltumorene og er lokalisert i subkutis i området for analsekkene, typisk i klokken 16 og 20 posisjon. Disse tumorene metastaserer ofte, og tidlig i forløpet, til den regionale lymfeknuten. Opptil cirka 50 % av hundene med denne kreftformen kan ha polydipsi og polyuri på grunn av paraneoplastisk hyperkalsemi. For øvrig kan nesten alle andre neoplasier som opptrer i huden også påvises perianalt (4, 5).
Utbyttet av den cytologiske undersøkelsen er i stor grad avhengig av kvaliteten på prøven, kompetansen til den som undersøker prøven, men også av lesjonen som sådan. Noen lesjoner er små og vanskelig å ta prøve fra eller er lokalisert til områder som ansikt og poter som er vanskelig å ta prøve fra uten at pasienten er sedert. Andre lesjoner kan ha nekrotiske og/eller inflammerte områder slik at prøven ikke er representativ for lesjonen. Stor grad av inngrepsblødning og/eller lav cellularitet i utstrykene kan også gi ikke-diagnostiske prøver (6). Cytologiske prøver fra perianalkjerteltumorer er ofte svært cellerike, med et høyt antall kjerneholdige celler i klumper og flak. Navnet hepatoid adenom kommer av likheten cellene har med hepatocytter. De har ofte rikelig med et granulert cytoplasma og en rund kjerne med stiplet kromatin og ofte en distinkt nukleole (2, 3). De fleste perianalkjerteltumorer er som sagt benigne, men cytologisk undersøkelse kan i regelen ikke sikkert utelukke en malign neoplasi fordi disse ikke alltid viser kriterier på malignitet cytologisk. Det ble nylig publisert et kasus hvor både cytologisk og histologisk undersøkelse viste en veldifferensiert perianalkjerteltumor som metastaserte (7). Derfor vil en, selv om den cytologiske diagnosen fremstår som sikker, i alle tilfeller anbefale å undersøke massen histologisk etter fjerning. Histologisk undersøkelse vil kunne ettervise tap av en organisert vevsarkitektur, invasjon i omliggende vev, og fokal proliferasjon av reserveceller ved malignitet, men den histologiske diagnosen gir heller ikke alltid et sikkert grunnlag for å predikere det videre forløpet.
Majoriteten av perianalkjerteladenomene hos intakte hannhunder angis å kunne behandles med kastrasjon, eventuelt i kombinasjon med kirurgi. Kirurgisk behandling er aktuelt i de tilfellene der tumor persisterer etter kastrasjon, tumor opptrer hos en tispe eller en kastrert hannhund, eller i tilfeller hvor kastrasjon ikke er ønsket eller tumor er ulcerert (4, 5)
Referanser
Blackwood L. Tumours of the skin and subcutaneous tissues. I: Dobson JM, Lascelles BDX, eds. BSAVA Manual of canine and feline oncology. 3rd ed. Gloucester: British Small Animal Veterinary Association, 2011:130-58.
Fisher DJ. Cutaneous and subcutaneous lesions I: Valenciano AC, Cowell RL, eds. Cowell and Tyler’s diagnostic cytology and hematology of the dog and cat. 4th ed. St. Louis, Missouri: Elsevier Mosby, 2014:80-109.
Raskin RE. Skin and subcutaneous tissues. I: Raskin RE, Meyer DJ, eds. Canine and feline cytology. A color atlas and interpretation guide. 3rd ed. St. Louis, Missouri: Elsevier, 2016:34-90.
Bray J. Tumours of the perianal region. I: Dobson JM, Lascelles BDX, eds. BSAVA Manual of canine and feline oncology. 3rd ed. Gloucester: British Small Animal Veterinary Association, 2011:223-8.
Turek MM, Withrow SJ. Perianal tumors. Cancer of the gastrointestinal tract. I: Withrow SJ, Vail DM, Page, RL, eds. Withrow & MacEwen’s small animal clinical oncology. 5th ed. St. Louis, Missouri: Elsevier Saunders, 2013:423-31.
Meinkoth JH, Cowell RL, Tyler RD. Cell types and criteria of malignancy. I: Valenciano AC, Cowell RL, eds. Cowell and Tyler’s diagnostic cytology and hematology of the dog and cat. 4th ed. St. Louis, Missouri: Elsevier Mosby, 2014:20-47.
McCourt MR, Levine GM, Breshears MA, Wall CR, Meinkoth JH. Metastatic disease in a dog with a well-differentiated perianal gland tumor. Vet Clin Pathol 2018;47: 649-53..